Новейший метод лечения неспецифического язвенного колита
Содержание статьи
Определена потенциально новая терапия болезни Крона и язвенного колита — Medical Insider
Автор Трусова Валентина Ивановна На чтение 4 мин. Опубликовано 11.03.2019 18:38
Обновлено 11.03.2019 16:23
Люди с воспалительным заболеванием кишечника (ВЗК) живут с частыми, короткими эпизодами болей в животе, диареи и в тяжелых случаях ректального кровотечения. В новом исследовании ученые обнаружили новый метод лечения воспалительных заболеваний кишечника. Результаты научной работы опубликованы в журнале Science Translational Medicine.
Традиционные методы лечения ВЗК
Традиционные методы лечения направлены на непосредственное подавление воспаления, но многим пациентам такое лечения не приносит облегчения. По данным авторов исследования, более 1 миллиона человек в Соединенных Штатах страдают от ВЗК, включая болезнь Крона и язвенный колит. Оба состояния характеризуются неконтролируемым воспалением, но в разных отделах желудочно-кишечного тракта. Как правило, они лечатся гормональными противовоспалительными препаратами, такими как кортикостероиды. В более серьезных случаях применяются сильные иммуносупрессоры, такие как ингибиторы ФНО, которые нейтрализуют важный иммунный белок. Иммунодепрессанты могут быть очень эффективными, но они имеют побочные эффекты, такие как повышенный риск инфекции и рака.
Материалы и методы обследования
Чтобы выделить гены, которые играют роль в возникновении ВЗК через невоспалительные пути, Стаппенбек с соавтором исследования Джерардом Кайко (Gerard Kaiko) проанализировали 1800 кишечных биоптатов из 14 независимых, общедоступных источников данных по ВЗК. Биопсия была получена из разных исследований, в которых пациенты с ВЗК по-разному сравнивались со здоровыми людьми. Образцы кишечного биоптата собирались у людей с тяжелой, средней и легкой степенью тяжести ВЗК как из воспаленных, так и здоровых участков кишечника. Чтобы проверить роль гена и его белка в воспалении кишечника, исследователи дали мышам химическое вещество, вызывающее воспаление кишечника, имитируя ВЗК, и безвредное химическое вещество для сравнения.
Результаты научной работы
Исследователи из Медицинской школы Вашингтонского университета (Washington University School of Medicine) в Сент-Луисе обнаружили соединение, которое может оказывать лечебный эффект на ВЗК без прямого воздействия на воспаление. Соединение снижает активность гена, связанного со свертыванием крови. Ученые обнаружили ген в местах воспаления и повреждения кишечника, и блокирование его активности уменьшает симптомы ВЗК у мышей. Примечательно, что этот ген особенно активен у людей с тяжелыми заболеваниями и у тех, кто не реагирует на сильнодействующие биологические препараты, известные как ингибиторы ФНО, которые назначают для лечения ВЗК тяжелой степени.
«Существует большой интерес к новым методам лечения ВЗК, так как противовоспалительная терапия помогает не всем больным», — сказал автор исследования Таддеус С. Стаппенбек (Thaddeus S. Stappenbeck). «Мы нашли уникальную мишень, блокирование которой уменьшает воспаление и признаки заболевания, по крайней мере, у мышей».
Анализ показал, что группа генов, связанных со свертыванием крови, задействована также при ВЗК. У людей с ВЗК вероятность возникновения тромбов в 2-3 раза выше, чем у населения в целом, причем риск особенно высок во время обострения. Исследователи сократили список генов до нескольких, которые играли роль как в воспалительных, так и в эпителиальных клетках. Особенно выделялся один: ген SERPINE-1. Этот ген и соответствующий ему белок были обнаружены при ВЗК. Оба они также участвуют в ранней стадии процесса свертывания крови, но ранее не были связаны с воспалением.
Мыши, которые получали вредное химическое вещество, теряли вес, в их кишечнике имелись признаки повреждения многими воспалительными клетками и белками, и ген SERPINE-1 был экспрессирован в 6 раз выше, чем у мышей, которые получали безвредное химическое вещество. Когда мышей с ВЗК-подобными симптомами лечили соединением под названием MDI-2268, которое блокировало активность белка, у них стабилизировался вес и снизилось воспаление в кишечнике, чем у мышей, которых лечили плацебо.
«Самое удивительное в этом то, что SERPINE-1 и его белок, по-видимому, сильнее экспрессируется у людей с тяжелой степенью ВЗК и у тех, кто не реагирует на иммунодепрессивные биологические препараты», — сказал Стаппенбек.
Авторы другого исследования утверждают, что женщины с воспалительным заболеванием кишечника подвержены большему риску психических заболеваний.
Источник
Озанимод: новое лекарство против язвенного колита и болезни Крона | МОСМЕДПРЕПАРАТЫ
«Бристол-Майерс Сквибб» (Bristol-Myers Squibb) отчиталась по результатам опорного клинического испытания, проверившего безопасность и эффективность лечения умеренно-тяжелого язвенного колита препаратом-кандидатом озанимод (ozanimod).
Продемонстрированная результативность лечения язвенного колита пероральным озанимодом не уступила эффективности, обеспечиваемой инъекционными биологическими лекарственными препаратами. Профиль безопасности озанимода характеризуется приличной переносимостью и отсутствием каких-либо серьезных побочных реакций.
Применимость озанимода в лечении язвенного колита может быть распространена и на терапию болезни Крона. Вскоре будут готовы результаты соответствующей заключительной клинической проверки.
Озанимод получен «Бристол-Майерс Сквибб» в результате поглощения «Селджен» (Celgene): сделка стоимостью 74 млрд долларов была закрыта в ноябре 2019 года.
Озанимод уже встал на коммерческие рельсы: в марте 2020 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило «Зепосиа» (Zeposia, озанимод) — новый лекарственный препарат для терапии рецидивирующих форм рассеянного склероза. В мае это же сделало Европейское агентство по лекарственным средствам (EMA), разрешившее применять «Зепосиа» в терапии рецидивирующе-ремиттирующего рассеянного склероза в активной форме.
Помимо озанимода «Бристол-Майерс Сквибб» разрабатывает еще одно лекарственное средство против патологий аутоиммунной природы, в том числе воспалительных заболеваний кишечника: деукравацитиниб (deucravacitinib) — первый в своем классе пероральный избирательный ингибитор тирозинкиназы 2 (TYK2). О нем «Мосмедпрепараты» подробно рассказывали в материале «Деукравацитиниб: лекарство будущего против аутоиммунных заболеваний».
Эффективность озанимода в лечении язвенного колита
Клиническое исследование TRUE NORTH (NCT02435992) фазы III (рандомизированное, двойное слепое, плацебо-контролируемое, многоцентровое, международное) охватило взрослых пациентов (n=645) с эндоскопически подтвержденным диагнозом язвенного колита в активной форме, протекающим с умеренно-тяжелой степенью выраженности. Под последней понимался трехкомпонентный общий балл клиники Мейо в пределах 6–12, включавший эндоскопический подбалл ≥ 2, подбалл ректальных кровотечений ≥ 1, подбалл частоты актов дефекации ≥ 1.
Участники придерживались стабильной терапии пероральными аминосалицилатами, преднизоном (≤ 20 мг/день) или мультиматриксным будесонидом.
Испытуемым ежедневно перорально назначали плацебо или 1 мг озанимода.
Исследование было поделено на два этапа: 10-недельная индукционная терапия, по завершении которой ответившие на лечение переходили к ослепленной 42-недельной поддерживающей терапии. Пациентов без ответа на лечение переводили в открытую группу поддерживающей терапии, в которой всем назначали только озанимод.
Первичная конечная точка была установлена пропорцией испытуемых, вышедших к клинической ремиссии, заявленной композитным клиническим и эндоскопическим баллом (на основе трехкомпонентного балла клиники Мейо): отсутствии ректальных кровотечений, подбалл частоты актов дефекации ≤ 1 (с уменьшением их абсолютного числа на ≥ 1), эндоскопический подбалл ≤ 1 (без контактной кровоточивости слизистой).
Среди вторичных конечных точек:
- клинический ответ: снижение общего трехкомпонентного балла клиники Мейо на ≥ 2 и ≥ 35%, снижение подбалла ректальных кровотечений на ≥ 1 или абсолютного их числа до ≤ 1;
- эндоскопическое улучшение: эндоскопический подбалл ≤ 1, причем без контактной кровоточивости слизистой;
- заживление слизистой: эндоскопическое улучшение на фоне гистологической ремиссии — отсутствие нейтрофилов в эпителиальных криптах или собственной пластинке слизистой оболочки, не повышенное число эозинофилов, отсутствует деформация крипт, нет эрозий, изъязвлений или грануляционной ткани;
- гистологическая ремиссия: согласно баллу по шкале Гебса (Geboes), которая имеет 6 градаций: 0 — только структурные изменения, 1 — хронический воспалительный инфильтрат, 2A — эозинофилы в собственной пластинке, 2B — нейтрофилы в собственной пластинке, 3 — нейтрофилы в эпителии, 4 — разрушение крипт, 5 — эрозии или изъязвления.
Индукционный этап: 10 недель лечения
Группа озанимода превзошла группу плацебо в задаче выхода к клинической ремиссии язвенного колита: таковая засвидетельствована для 18,4% участников — против 6,0% (p<0,0001). Указанное не зависело от того, получали ли ранее пациенты ингибиторы фактора некроза опухоли (TNF) или нет.
Получавшие озанимод также подтвердили вторичные конечные точки:
- клинический ответ: 47,8% — против 25,9% (p<0,0001);
- эндоскопическое улучшение: 27,3% — против 11,6% (p<0,0001);
- заживление слизистой: 12,6% — против 3,7% (p<0,001).
Поддерживающий этап: 52 недели лечения
Назначение озанимода обеспечило выход к клинической ремиссии язвенного колита среди 37,0% испытуемых — против 18,5% в группе плацебо (p<0,0001). Указанное не зависело от того, прежде получали ли пациенты TNF-ингибиторы или нет.
При этом сохраненная ремиссия — та, которая зафиксировалась после 10-недельного курса лечения, и затем осталась по прошествии еще 42 недель лечения, — отмечена у 51,9% больных против 29,3% (p=0,0047).
Статус клинической ремиссии язвенного колита без сопутствующего применения кортикостероидов (без их использования на протяжении не менее чем 12 недель) отказался справедливым для 31,7% пациентов, придерживающихся терапии озанимодом, — против 16,7% в контрольной группе (p<0,001).
Статус устойчивой ремиссии язвенного колита — ремиссия по прошествии 10 и 52 недель лечения среди всех испытуемых, перешедших к поддерживающему этапу терапии, — продемонстрирован у 17,8% против 9,7% (p=0,003).
Группа озанимода также подтвердила вторичные конечные точки:
- клинический ответ: 60,0% — против 41,0% (p<0,0001);
- эндоскопическое улучшение: 45,7% — против 26,4% (p<0,001);
- заживление слизистой: 29,6% — против 14,1% (p<0,001).
Безопасность озанимода в лечении язвенного колита
На индукционном этапе лечения язвенного колита наиболее распространенными побочными реакциями в ответ на назначение озанимода были следующие: анемия (у 4,2% пациентов — против 5,6% в группе плацебо), назофарингит (3,5% против 1,4%), головная боль (3,3% против 1,9%).
На поддерживающем этапе профиль безопасности выглядел так: повышенный уровень аланинаминотрансферазы (АЛТ) [4,8% против 0,4%; без серьезных событий], головная боль (3,5% против 0,4%).

Эффективность озанимода при длительном лечении язвенного колита
Долгосрочное наблюдение за участниками клинического исследования TOUCHSTONE (NCT01647516) фазы II продемонстрировало, что многолетнее применение озанимода в ходе лечения язвенного колита выводит приблизительно 40% пациентов к клиническому ответу и/или клинической ремиссии заболевания.

Эффективность озанимода в лечении болезни Крона
«Бристол-Майерс Сквибб» продолжает проверку озанимода в лечении умеренно-тяжелой болезни Крона среди взрослых пациентов, заболевание которых адекватно не реагирует (или потеряло ответ) при назначении кортикостероидов, иммуномодуляторов и/или биологических препаратов. Для этого осуществляется опорная клиническая программа YELLOWSTONE, включающая клинические испытания фазы III: NCT03440372 и NCT03440385 — для оценки 12-недельной индукционной эффективности озанимода, NCT03464097 — 52-недельной поддерживающей эффективности.
Среди клинических и эндоскопических критериев включения: индекс активности болезни Крона (CDAI) в диапазоне от 220 до 450 баллов, усредненная частота ежедневных актов дефекации ≥ 4 и/или балл абдоминальной боли ≥ 2, балл простого эндоскопического индекса активности болезни Крона (SES-CD) ≥ 6 (или ≥ 4 при изолированном подвздошнокишечном заболевании).
Об успехах озанимода в лечении умеренно-тяжелой болезни Крона можно судить по результатам клинического исследования NCT02531113 фазы II, в котором 12-недельный терапевтический курс обеспечил эндоскопический ответ (уменьшение балла SES-CD хотя бы на 50%) у 23,2% участников, притом что индекс CDAI снизился в среднем на 130 пунктов.

Озанимод и лечение воспалительных заболеваний кишечника: механизм действия
Один из подходов к терапии воспалительных заболеваний аутоиммунной природы отталкивается от таргетирования лиганд-рецепторной системы сфингозин-1-фосфата (S1P) в целях модулирования аутоиммунных реакций.
Сфингозин-1-фосфат — липидно-сигнальная молекула, регулирующая ряд биологических процессов посредством своего взаимодействия с семейством рецепторов, сопряженных с G-белком (GPCR). Сфингозин-1-фосфат связывается с пятью таковыми (S1PR1–5), каждый из которых характеризуется, во-первых, разной экспрессией в тканях и, во-вторых, разными оказываемыми физиологическими эффектами, запускаемыми при активации S1P-лигандом.
- Рецептор 1 сфингозин-1-фосфата (S1PR1) экспрессирует на T- и B-лимфоцитах, астроцитах и нейронах, клетках эндотелия сосудов и кардиомиоцитах. Рецептор 5 сфингозин-1-фосфата (S1PR5) экспрессирует на естественных киллерах, олигодендроцитах и клетках эндотелия сосудов.
Сфингозин-1-фосфат отвечает за важную сигнализацию, необходимую для выхода лимфоцитов из лимфоидных органов в системное русло. Если осуществить соответствующую модуляцию сигнального пути S1P, можно добиться удержания лимфоцитов в лимфоузлах с результирующим ослаблением воспалительных процессов.
Так как в патофизиологии воспалительных заболеваний кишечника особая роль отводится лимфоцитам — B- и T-клеткам, атакующим желудочно-кишечный тракт, имеет смысл снизить их присутствие в нем. При язвенном колите и болезни Крона провоспалительные лимфоциты, ненадлежащим образом активированные, покидают лимфоидную ткань, мигрируя в кишечник, где способствуют хроническому воспалению. Поскольку с таковым ассоциирован повышенный уровень сфингозин-1-фосфата, имеет смысл нацелиться на его сигнальный путь, чтобы заблокировать градиентно-зависимую (из областей с низким градиентом в области с высоким) миграцию лимфоцитов.
Озанимод (ozanimod) — пероральный низкомолекулярный избирательный агонист рецепторов 1 и 5 сфингозин-1-фосфата (S1PR1 и S1PR5). Иммуномодулирующий механизм действия озанимода обусловлен интернализацией S1P-рецепторов с их последующей деградацией (функциональный антагонизм) в убиквитин-протеасомном метаболическом пути. Это приводит к сдерживанию миграции определенного подтипа активированных лимфоцитов (T-хелперов CD4+ CCR7+ и T-киллеров CD8+ CCR7+) из лимфоидной ткани к местам воспаления. При этом сохраняется целостность иммунологического надзора над инфекциями и опухолями, так как S1P-сигнализация не затрагивает подмножество лимфоцитов, которые не мигрируют через лимфоидную ткань.
 Упрощенно говоря, озанимод секвестирует (направляет) лимфоциты в периферические лимфоидные органы, устраняя их из областей хронического воспаления.
Упрощенно говоря, озанимод секвестирует (направляет) лимфоциты в периферические лимфоидные органы, устраняя их из областей хронического воспаления.
- К слову, озанимод нашел себя в терапии рассеянного склероза по двум причинам. Во-первых, он, связываясь с S1PR1 на лимфоцитах, препятствует их миграции в центральную нервную систему, обеспечивая противовоспалительный эффект. Во-вторых, озанимод связывается с S1PR1 и S1PR5 на астроцитах и олигодендроцитах соответственно, модулируя разрушительную клеточную активность и сдерживая ухудшение неврологических функций, ассоциированных с рассеянным склерозом: за счет подавления воспалительных цитокинов и процессов димиелинизации и потери аксонов, а также сохранения ГАМК-эргической передачи.
Озанимод для лечения язвенного колита и болезни Крона: конкурентные позиции
Если «Бристол-Майерс Сквибб» сумеет довести до конца разработку озанимода против язвенного колита и болезни Крона, по итогам заручившись соответствующим регуляторным одобрением, врачебное и пациентское сообщества получат новое лекарственное средство, выгодно позиционируемое в условиях напряженной конкурентной борьбы с уже существующими препаратами.
Озанимод характеризуется тройкой примечательных особенностей. Во-первых, его эффективность не уступает той, которую предоставляют биологические препараты и низкомолекулярные ингибиторы Янус-киназ (JAK). Список лекарственных средств, одобренных в терапии воспалительных заболеваний кишечника умеренно-тяжелой выраженности, включает следующие:
- антиинтегрины: «Тизабри» (Tysabri, натализумаб) — блокатор α4-интегрина, «Энтивио» (Entyvio, ведолизумаб) — блокатор α4β7-интегрина;
- ингибиторы фактора некроза опухоли (TNF): «Хумира» (Humira, адалимумаб), «Симпони» (Simponi, голимумаб) и «Ремикейд» (Remicade, (инфликсимаб);
- антагонисты интерлейкина: «Стелара» (Stelara, устекинумаб) — ингибитор интерлейкина 12 (IL-12) и интерлейкина 23 (IL-23);
- ингибиторы Янус-киназ (JAK): «Зелджанс»/«Яквинус» (Xeljanz/Jakvinus, тофацитиниб) — ингибитор Янус-киназ 1, 2 и 3 (JAK1, JAK2 и JAK3).
Во-вторых, профиль безопасности озанимода характеризуется приемлемой переносимостью, не требующей дополнительных предупреждений о рисках серьезных или жизнеугрожающих побочных реакциях.
В-третьих, озанимод сделан в пероральной рецептуре, тогда как все прочие из указанных выше препаратов (кроме JAK-ингибиторов) реализованы в не особо удобной инъекционной подкожной или внутривенной формуляции.

Дополнительные материалы
UEGW 2020. Investor Presentation. Bristol-Myers Squibb. [PDF]
Ozanimod Induction and Maintenance Treatment for Ulcerative Colitis. N Engl J Med. 2016 May 5;374(18):1754-62. [PDF]
Ozanimod induction therapy for patients with moderate to severe Crohn’s disease: a single-arm, phase 2, prospective observer-blinded endpoint study. Lancet Gastroenterol Hepatol. 2020 Sep;5(9):819-828. [PDF]
Sphingosine-1-Phosphate Signaling in Inflammatory Bowel Disease. Trends Mol Med. 2017 Apr;23(4):362-374. [PDF]
Ozanimod (RPC1063) is a potent sphingosine‐1‐phosphate receptor‐1 (S1P1) and receptor‐5 (S1P5) agonist with autoimmune disease‐modifying activity. Br J Pharmacol. 2016 Jun; 173(11): 1778–1792. [PDF]
Источник
симптомы НЯК, чем лечить неспецифический язвенный колит в статье проктолога Куракина А. А.
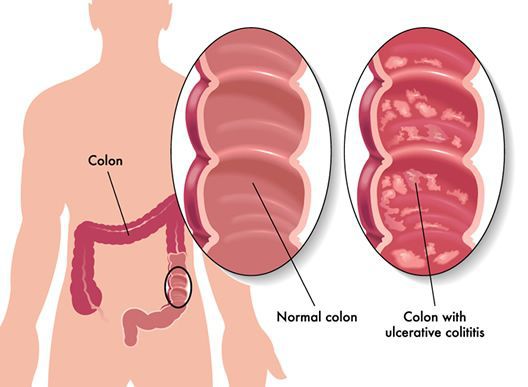
Неспецифический язвенный колит (или просто язвенный колит) — хроническое воспаление толстой кишки аутоиммунного характера. Данное заболевание относится к группе воспалительных заболеваний толстого кишечника.
Эпидемиология
Заболевание преобладает в развитых странах Европы и Северной Америки. Язвенный колит встречается в 20-260 случаев на 100 000 человек. С каждым годом число заболевших увеличивается.[2]
Чаще всего болеют лица в возрасте от 21 до 42 лет, а также пациенты после 54 лет. Самые опасные периоды в развитии язвенного колита — это первый год болезни (из-за быстрого развития воспаления при фульминантном течении появляются осложнения, опасные для жизни) и десятый год (за этот период развиваются злокачественные новообразования).
Факторы риска до сих пор до конца не изучены. Существует следующая закономерность:
- Взаимосвязь курения и язвенного колита. По статистическим данным курящие люди реже болеют язвенным колитом.
- Аппендэктомия (удаление аппендицита) в анамнезе снижает заболеваемость язвенным колитом.
- Снижение количества пищевых волокон способствует появлению болезни.
- Лица, чаще болеющие детскими инфекциями, имеют склонность к появлению данного заболевания.
Этиология
Происхождение язвенного колита на сегодняшний день неизвестно. Существуют следующие теории развития заболевания:
- Язвенный колит возникает под действием определённых экзогенных (внешних) факторов, которые не известны. Предположительной причиной является инфекция.
- Заболевание имеет аутоиммунный характер. Существует наследственная предрасположенность к развитию болезни. Под воздействием определённых факторов запускаются иммунные реакции, вырабатываются антитела, направленные на клетки толстого кишечника.
- Язвенный колит развивается вследствие реакции организма на определённые продукты питания, при этом воспаляется кишечная стенка.
Первые признаки заболевания: кровь и слизь в стуле, диарея, боли в животе, повышение температуры тела.
Основными симптомами неспецифического язвенного колита кишечника являются:
- кишечные кровотечения;
- диарея;
- запор;
- боль в животе;
- тенезмы (ощущение постоянных режущих, тянущих, жгучих болей в толстой кишке — позывов к дефекации, однако при этом выделение кала не происходит);
- лихорадка;
- снижение массы тела;
- тошнота, рвота;
- слабость;
- внекишечные симптомы (артрит, узловатая эритема, увеит и другие).
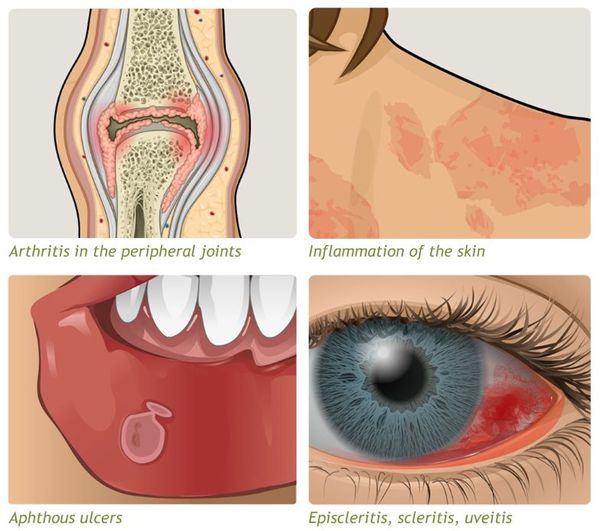
Заболевание хроническое — симптомы возникают только при обострении, при ремиссии их может не быть.
Характер преобладающей симптоматики зависит от тяжести заболевания и вовлечённого в воспалительный процесс отдела толстого кишечника. Например, при тотальном поражении наблюдается частый жидкий стул с большим количеством крови в кале, боли в животе спастического характера. При тяжёлом течении присоединяются симптомы общей интоксикации (лихорадка, тошнота, рвота, слабость).
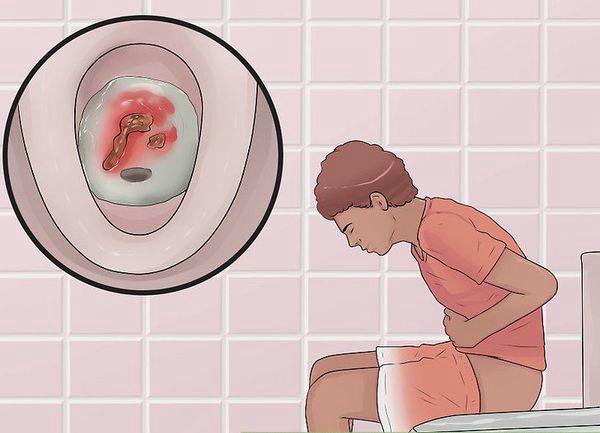
При поражении дистальных отделов толстого кишечника (проктит) чаще возникает запор, ложные позывы на дефекацию, тенезмы, в кале обнаруживаются следы алой крови, слизи или гноя. Для оценки тяжести язвенного колита предложены критерии Truelove и Witts.
При язвенном колите происходит каскад воспалительных реакций. В результате воздействия триггерного (инициирующего) фактора стимулируются Т- и В-лимфоциты, что, в свою очередь, приводит к образованию иммуноглобулинов М и G. Дефицит Т-супрессоров усиливает аутоиммунный ответ. Образование иммуноглобулинов М и G приводит к появлению иммунных комплексов и активации сиcтемы комплемента, который обладает цитотоксическим действием. В очаг воспаления проникают нейтрофилы и фагоциты, при этом высвобождаются медиаторы воспаления.
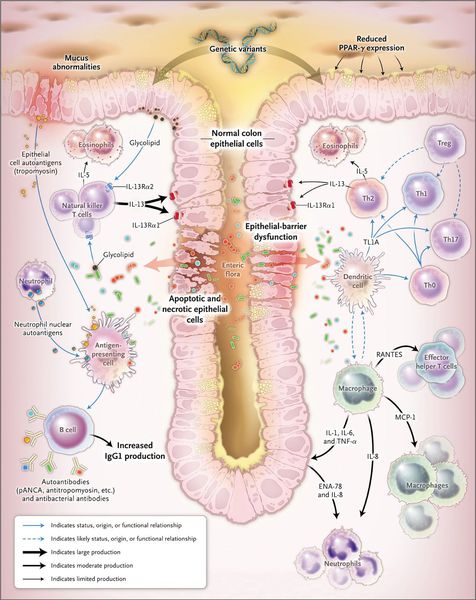
Одним из механизмов патогенеза язвенного колита является нарушение барьерной функции слизистой оболочки толстой кишки и регенераторной функции.
Реакция организма на стресс с патологическим нейрогуморальным ответом приводит к активизации аутоиммунного процесса. Часто больные язвенным колитом имеют эмоциональную нестабильность.
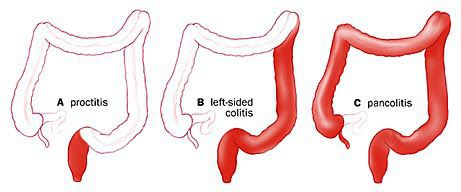
По распространённости процесса различают:
- проктит (с вовлечением прямой кишки);
- левосторонний колит (поражение прямой сигмовидной и нисходящей ободочной кишки);
- тотальный колит (поражение всех отделов толстого кишечника).
По степени тяжести течения:[3]
- лёгкое течение;
- среднетяжёлое течение;
- тяжёлое течение.
По характеру течения:
- острое течение (менее 6 месяцев от начала болезни);
- фульминантное (быстро развивающееся);
- постепенное;
- хронический язвенный колит непрерывного течения (периоды ремиссии (ослабления симптомов) менее 6 месяцев при правильном лечении);
- хронический язвенный колит рецидивирующего течения (периоды ремиссии более 6 месяцев): редко рецидивирующее (один раз в год или меньше) или часто рецидивирующее (более 2 раз в год).
Язвенный колит — это хроническое заболевание, при котором бывают периоды, когда возникает обострение и периоды, когда симптомы затухают или не выявляются — стадия ремиссии. Язвенный колит может обостряться без явной причины, однако чаще это происходит под воздействием стресса, неправильного питания и приёме некоторых лекарств.
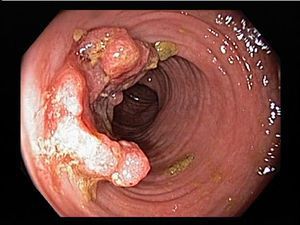
Местные осложнения
К местным осложнениям относятся:
- перфорация;
- токсическая дилатация (расширение) толстого кишечника;
- обильное кишечное кровотечение;
- колоректальный рак.
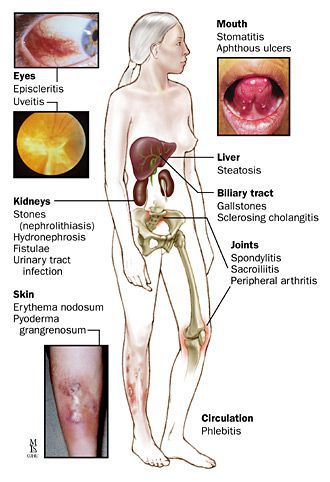
Системные осложнения
Проявляются внекишечными симптомами, причина которых до сих пор не изучена. Чаще поражаются ротовая полость, кожа, суставы.
К системным осложнениям относятся:
- узловатая эритема (поражение кожи и подкожной клетчатки);
- гангренозная пиодермия (поражение кожи крупными болезненными язвами);
- эписклерит (поражение эписклеральной ткани глаза);
- артропатия (поражение суставов);
- анкилозирующий спондилит (воспаление суставов позвоночника);
- поражения печени (повышение трансаминаз крови, гепатомегалия);
- первичный склерозирующий холангит (сужение просвета желчных протоков в результате воспаления).
При диагностике в первую очередь оценивается клиника заболевания, анамнез, производится осмотр с обязательным пальцевым исследованием прямой кишки.
Наиболее важными в диагностике язвенного колита являются эндоскопические методы исследования: ректороманоскопия, колоноскопия с биопсией. Так же для уточнения диагноза применяются ирригоскопия, МСКТ-колоноскопия.
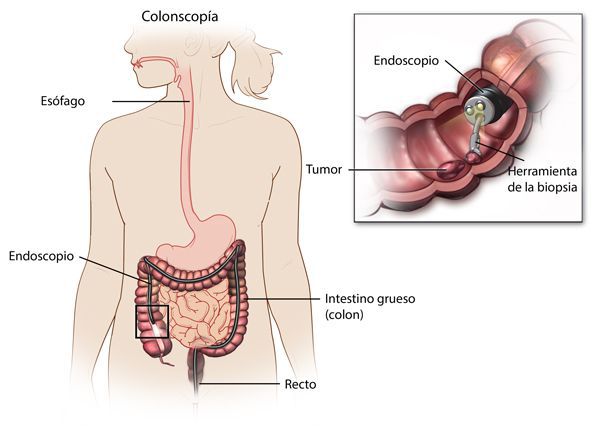
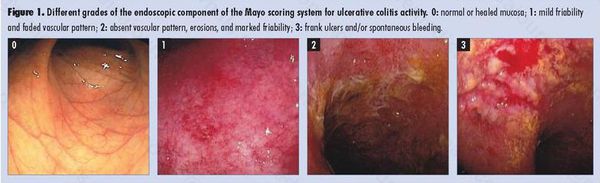
По эндоскопической картине можно определить степень воспаления толстого кишечника. Существуют четыре степени воспаления кишечника:
- При I степени наблюдается отёчность слизистой оболочки, гиперемия, сглаженность или отсутствие сосудистого рисунка, определяются точечные кровоизлияния, слизистая ранима, контактно кровоточит.
- При II степени добавляется зернистость, могут присутствовать эрозии, фиброзный налёт на стенках кишки.
- При III степени эрозии сливаются между собой, образуются язвы, в просвете кишки гной и кровь.
- При IV степени, помимо вышесказанного, появляются псевдополипы, состоящие из грануляционной ткани.
Язвы не проникают глубже подслизистого слоя.
При рентгенологическом исследовании определяется:
- отсутствие гаустр (мешкообразных выпячиваний стенки толстой кишки);
- сглаженность контуров;
- изъязвления, отёк, зубчатость, двойной контур;
- утолщение слизистой и подслизистой оболочек;
- преимущественно продольные и грубые поперечные складки;
- воспалительные полипы.
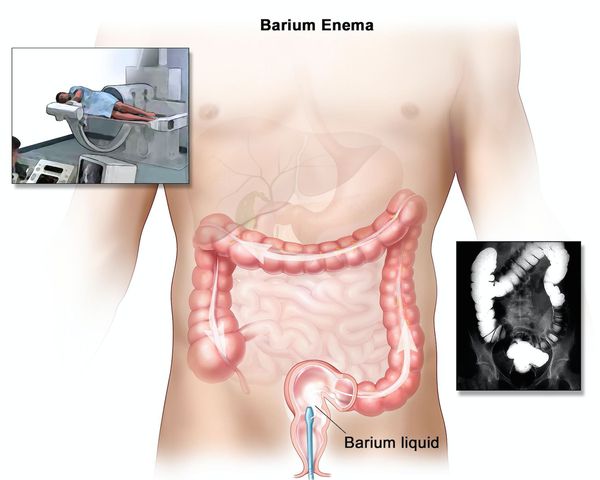
Ирригоскопия помогает не только в диагносте язвенного колита, но и в выявлении серьёзных осложнений, таких как токсическая дилатация (чрезмерное расширение просвета толстой кишки).
Дифференциальный диагноз:
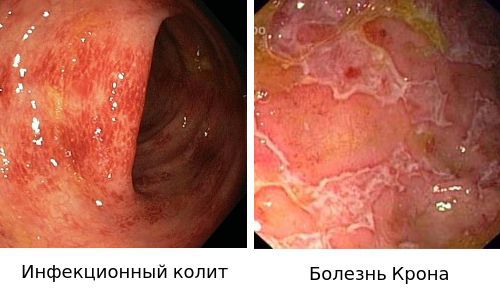
- Для подтверждения диагноза «Инфекционный колит» используют бактериологическое исследование.
- Диагноз «Болезнью Крона» ставится на основании эндоскопической картины и гистологического исследования биоптата слизистой.
- Ишемический колит.
Тактика зависит от локализации поражения и тяжести течения. При дистальных формах заболевания течение обычно лёгкое, поэтому больные могут лечиться в амбулаторных условиях. Тотальное или левостороннее поражение чаще имеет тяжёлое течение, поэтому требует госпитализации и лечения в условиях стационара.
Диета
Назначаются диеты № 4, 4Б, 4В по Певзнеру. Цель диеты — уменьшить воспаление, бродильные и гнилостные процессы в кишечнике, нормализовать функции кишечника и других органов пищеварения. Блюда жидкие, полужидкие, протёртые, сваренные в воде или на пару. Исключены очень горячие и холодные блюда.
Разрешённые при язвенном колите продукты:
- сухари, супы слизистой консистенции, сваренные на обезжиренном мясном, рыбном бульоне или овощном отваре, с хорошо проваренными крупами, лапшой или вермишелью, допускается добавление фрикаделек;
- нежирное мясо и рыба;
- тщательно проваренные каши;
- фруктовые пюре;
- свежий протёртый творог;
- сахар в маленьких дозах;
- желе и кисели из черники, кизила, черемухи, айвы, груш;
- крепкий черный чай, можно с лимоном, отвар из шиповника, черной смородины, черники и черемухи;
- паровой омлет, яйца, сваренные вкрутую; сливочное масло.
Запрещенные при язвенном колите продукты:
- сдоба и кондитерские изделия;
- чёрный хлеб;
- мясные и рыбные жирные бульоны;
- колбасы, солёная и копчёная рыба, консервы;
- алкоголь;
- кофе;
- молоко;
- газированные сладкие напитки;
- свежие овощи и фрукты;
- перловая и пшеничная каши, бобовые.
Консервативная терапия
К консервативной терапии относятся:
- аминосалицилаты, препараты 5-аминосалициловой кислоты (5-АСК, месалазин);
- кортикостероиды;
- иммунодепрессанты;
- билогическая терапия.
Аминосалицилаты являются препаратами первой линии и применяются в первую очередь. Для купирования атаки язвенного колита обычно требуется 3-6 недель терапии по 1-2 г/кг в сутки. После этого проводится противорецидивное лечение сульфасалазином (3 г/сут) или месалазином (2 г/сут).
При дистальном поражении (проктит) отдаётся предпочтение формам препарата в виде свечей. При левостороннем поражении — препаратам в форме пены для ректального применения. При тотальном поражении используют таблетированные формы препаратов.
При лечении данными препаратами ремиссия достигается в 74-81 % случаев.
Наиболее выраженным и эффективным противовоспалительным средством являются глюкокортикоиды.
Основными показаниями для лечения глюкокортикоидами являются:
- острое течение тяжёлой и среднетяжёлой степени;
- тяжёлое или среднетяжёлое левостороннее и тотальное поражение при наличии III степени воспаления по данным эндоскопического исследования;
- неэффективность или недостаточная эффективность лечения аминосалицилатами при хроническом течении заболевания.
При остром тяжёлом течении назначают внутривенное введение глюкокортикоидов (преднизолона не менее 120 мг/сут) 4-6 раз в день. Обязательно проводится коррекция водно-электролитного баланса, переливание компонентов крови, гемосорбция. Через неделю после внутривенного введения переходят на приём преднизолона внутрь. За это время проводится гастроскопия для исключения язвенной болезни желудка и двенадцатиперстной кишки.
При среднетяжёлой форме можно ограничиться пероральным приёмом преднизолона. Обычно преднизолон назначается в дозе 1,5-2 мг/кг массы тела в сутки. Максимальная доза 100 мг (у лиц пожилого возраста 60 мг).
Если отсутствуют побочные эффекты, то приём продолжают ещё 10-14 дней, затем снижают дозу на 10 мг каждые 10 дней. С 30-40 мг переходят на однократный приём преднизолона. С 30 мг дозу снижают по 5 мг в неделю. Обычно курс гормональной терапии составляет от 8 до 12 недель. Параллельно с гормонотерапией применяют аминосалицилаты до полной отмены гормонов.
При проктите применяются глюкокортикоиды ректально в микроклизмах. ?