Неспецифический язвенный колит у детей литература
Содержание статьи
Неспецифический язвенный колит у детей. Симптомы. Диагностика. Лечение.
Неспецифический язвенный колит — хроническое воспалительно-дистрофическое заболевание толстой кишки с рецидивирующим либо непрерывным течением, местными и системными осложнениями.
Неспецифический язвенный колит распространён преимущественно среди населения индустриально развитых стран (распространённость среди взрослых — 40-117:100 000). У детей он развивается относительно редко, составляя 8-15% от заболеваемости взрослых. В последние два десятилетия наблюдают рост числа больных неспецифическим язвенным колитом как среди взрослых, так и среди детей всех возрастных групп. Дебют заболевания может возникнуть даже в грудном возрасте. Распределение по полу составляет 1:1, причём в раннем возрасте чаще болеют мальчики, в подростковом — девочки.
Этиология и патогенез
Несмотря на многолетнее изучение этиология заболевания остаётся невыясненной. Среди различных теорий развития неспецифического язвенного колита наибольшее распространение получили инфекционная, психогенная и иммунологическая. Поиски какой-либо единой причины возникновения язвенного процесса в толстой кишке до сих пор безуспешны. В качестве этиологических факторов предполагают вирусы, бактерии, токсины, некоторые ингредиенты пищи, способные, как триггеры, вызвать начало патологической реакции, приводящей к повреждению слизистой оболочки кишки. Большое значение придают состоянию нейроэндокринной системы, местной иммунной защите слизистой оболочки кишки, генетической предрасположенности, неблагоприятным факторам внешней среды, психологическим стрессам, ятрогенно-медикаментозным воздействиям. При неспецифическом язвенном колите возникает каскад самоподдерживающихся патологических процессов: сначала неспецифических, затем аутоиммунных, повреждающих органы-мишени.
Классификация
Современная классификация неспецифического язвенного колита учитывает протяжённость процесса, выраженность клинических симптомов, наличие рецидивов, эндоскопические признаки.
Рабочая классификация неспецифического язвенного колита
Локализация | Активность | Течение | Фаза | Степень |
Дистальный колит Левосторонний колит Тотальный колит Внекишечные проявления и осложнения | Минимальная Умеренная Резко выраженная | Молниеносное Острое Хроническое • рецидивирующее • непрерывное | Ремиссия Обострение | Лёгкая Среднетяжёлая Тяжёлая |
Клиническая картина
Клиническая картина представлена тремя ведущими симптомами: диареей, выделением со стулом крови, болями в животе. Почти в половине случаев заболевание начинается исподволь. При лёгком колите заметны единичные прожилки крови в стуле, при тяжёлом — значительная её примесь. Иногда стул приобретает вид зловонной жидкой кровавой массы. У большинства больных развивается диарея, частота стула варьирует от 4-8 до 16-20 раз в сутки и более. В жидком стуле помимо крови содержатся в большом количестве слизь и гной. Диарею с примесью крови сопровождают, а иногда и предшествуют ей боли в животе, чаще во время еды или перед дефекацией. Боли схваткообразные, локализуются в низу живота, в левой подвздошной области или вокруг пупка. Изредка развивается дизентериеподобное начало болезни. Весьма характерны для тяжёлого неспецифического язвенного колита повышение температуры тела (обычно не выше 38 °С), снижение аппетита, общая слабость, снижение массы тела, анемия, задержка полового развития.
Осложнения неспецифического язвенного колита бывают системными и местными.
Системные осложнения многообразны: артриты и артралгии, гепатиты, склерозирующий холангит, панкреатиты, тяжёлые поражения кожи, слизистых оболочек (узловатая эритема, пиодермии, трофические язвы, рожистое воспаление, афтозный стоматит, пневмония, сепсис) и глаз (увеит, эписклерит).
Местные осложнения у детей развиваются редко. К ним относят профузное кишечное кровотечение, перфорацию кишки, острую токсическую дилатацию или стриктуру толстой кишки, поражение аноректальной области (трещины, свищи, абсцессы, геморрой, слабость сфинктера с недержанием кала и газов), рак толстой кишки.
Лабораторные и инструментальные исследования
При анализе крови обнаруживают лейкоцитоз с нейтрофилёзом и сдвигом лейкоцитарной формулы влево, снижение содержания эритроцитов, гемоглобина, сывороточного железа, общего белка, диспротеинемию со снижением концентрации альбумина и повышением у-глобулинов; возможны нарушения электролитного состава крови. Соответственно остроте и фазе заболевания повышаются СОЭ и концентрация С-реактивного белка.
Решающую роль в диагностике неспецифического язвенного колита играют эндоскопические методы исследования. При колоноскопии в начальный период болезни слизистая оболочка гиперемирована, отёчна, легкоранима. В дальнейшем формируется картина типичного эрозивно-язвенного процесса. В период манифестных проявлений циркулярные складки слизистой оболочки утолщаются, нарушается деятельность сфинктеров толстой кишки. При длительном течении заболевания складчатость исчезает, просвет кишки становится трубкообразным, её стенки — ригидными, анатомические изгибы сглаживаются. Нарастают гиперемия и отёк слизистой оболочки, появляется её зернистость. Сосудистый рисунок не определяется, выражена контактная кровоточивость, обнаруживают эрозии, язвы, микроабсцессы, псевдополипы.
Рентгенологически выявляют нарушение гаустрального рисунка кишки: асимметрию, деформацию или полное его исчезновение. Просвет кишки имеет вид шланга с утолщёнными стенками, укороченными отделами, сглаженными анатомическими изгибами.
Диагностика и дифференциальная диагностика
Диагноз устанавливают на основании клинико-лабораторных данных, результатов ректороманоскопии, сигмо- и колоноскопии, ирригографии, а также гистологического исследования биопсийного материала.
Дифференциальную диагностику проводят с болезнью Крона, целиакией, дивертикулитом, опухолями и полипами толстой кишки, туберкулёзом кишечника, болезнью Уиппла и др.
Лечение
Наибольшее значение в лечении неспецифического язвенного колита у детей придают диете. Назначают безмолочный стол № 4 по Певзнеру, обогащенный белком за счёт мясных и рыбных продуктов, яиц.
Основу базисной лекарственной терапии составляют сульфасалазин и препараты 5-аминосалициловой кислоты (месалазин). Их можно принимать через рот и вводить в виде лечебных клизм или свечей в прямую кишку. Дозу препаратов и длительность лечения определяют индивидуально. При тяжёлом течении неспецифического язвенного колита дополнительно назначают глюкокортикоиды. По строгим показаниям применяют иммунодепрессанты (азатиоприн). Проводят также симптоматическую терапию и местное лечение (микроклизмы).
Альтернативой консервативному лечению служит оперативное — субтотальная резекция кишки с наложением илеоректального анастомоза.
Профилактика
Профилактика направлена прежде всего на предупреждение рецидивов. После выписки из стационара всем больным следует рекомендовать курсы поддерживающего и противорецидивного лечения, включающего базисную медикаментозную терапию, диету и охранительно-восстановительный режим. Больные неспецифическим язвенным колитом подлежат обязательному диспансерному наблюдению. Профилактическую вакцинацию проводят только по эпидпоказаниям ослабленными вакцинными препаратами. Детей освобождают от экзаменов, физических нагрузок (занятий физкультурой, трудовых лагерей и т.д.). Обучение желательно проводить на дому.
Прогноз
Прогноз для выздоровления неблагоприятный, для жизни — зависит от тяжести болезни, характера течения, наличия осложнений. Показан регулярный контроль изменений слизистой оболочки толстой кишки из-за возможности её дисплазии.
Источник: Детские болезни. Баранов А.А. // 2002.
Источник
Неспецифический язвенный колит у детей

Неспецифический язвенный колит — заболевание, спровоцированное воспалительными процессами в толстом кишечнике. Чаще симптомы патологии диагностируют у пациентов в возрасте 15 — 30 лет и людей старше 60. Несмотря на такие возрастные рамки, диагноз «неспецифический язвенный колит» нередко ставят в детском возрасте. В статье рассматриваем специфику протекания НЯК у детей, методы лечения и прогнозируемые результаты терапии.
Содержание:
- Группа риска
- Почему дети заболевают НЯК
- Можно ли вылечить неспецифический язвенный колит
- Что делать, если ребенку поставили диагноз НЯК
- Язвенный колит и лечение препаратами
- На что жалуется ребенок
- Другие особенности симптоматики
- Классификация заболевания
- Диагностические мероприятия при НЯК
- Прогнозы
Группа риска
Согласно данным проведенных исследований, неспецифический язвенный колит чаще диагностируют у мужчин 25-29 лет. Женщины заболевают в период 15-19 лет. Люди в возрасте 55-65 лет находятся во второй уязвимой возрастной группе.
Этиология заболевания до конца не изучена, но считается, что воспалительные процессы могут спровоцировать такие факторы:
- Инфекции (бактериальные и вирусные патогены);
- Длительный прием оральных контрацептивов;
- Продолжительная гормональная терапия;
- Увлечение некоторыми видами диет;
- Курение.
Прослеживается взаимосвязь между повышенными рисками развития НЯК на фоне длительной терапии противовоспалительными препаратами нестероидного типа. Неспецифический язвенный колит у ребенка или взрослого появляется из-за пагубного действия на ЖКТ медикаментов, вызывающих в качестве побочных явлений пищевые аллергии.
Спровоцировать НЯК могут: перенесенный в детском возрасте паротит, расовая предрасположенность (доказано, что заболеванию подвержены люди белой расы, особенно еврейской национальности), отказ от курения (при условии, что у курильщика большой стаж).
Почему дети заболевают НЯК
НЯК — патология, по принципу развития и клинической картине схожая с болезнью Крона. От других ВЗК ее отличает чередование стадий ремиссии и обострения.
Достоверно неизвестно, почему дети разного возраста страдают от патологии КТ, но негласно гастроэнтерологи склоняются к генетической предрасположенности, как к основному фактору риска.
Немаловажную роль играют внешние факторы. Колит связывают с агентами извне, которые, попадая в ЖКТ, провоцируют воспаления в толстой кишке.
Распространенность НЯК — в пределах 41-116 случаев на 100 тыс. человек. Большой показатель летальных исходов отмечается, если симптомы неспецифического язвенного колита у детей появляются в выраженной форме, а заболевание при этом протекает молниеносно. При таких сценариях в кишечнике в течение года образуются злокачественные новообразования.
Можно ли вылечить неспецифический язвенный колит
Лечение неспецифического язвенного колита производится с целью устранить симптомы, беспокоящие ребенка, нормализовать естественные процессы в ЖКТ и продлить состояние ремиссии. НЯК считается хронической патологией кишечника, поэтому ни один врач не может гарантировать абсолютный успех терапевтического эффекта или спрогнозировать следующий рецидив.
Для колита характерно циклическое течение: периоды обострения патологии чередуются со спокойной фазой, которая может длиться месяцами.
Помимо лечения язвенного колита препаратами, важную роль играет строгий рацион питания. В остром периоде при НЯК рекомендована категоричная диета, в моменты ремиссии — более мягкая.
Что делать, если ребенку поставили диагноз НЯК
В первую очередь, родители детей с диагнозом «НЯК» должны осознать всю серьезность ситуации. Доскональное соблюдение рекомендаций лечащего врача и следование принципам диетического питания помогут устранить болезненные симптомы у ребенка и поспособствуют стабилизации состояния.
Питание при колите у детей предусматривает контроль баланса минералов и витаминов в продуктах из ежедневного рациона. Важно: превышение допустимых норм потребления жирной пищи и углеводосодержащих продуктов во время ремиссии может спровоцировать новый рецидив.
Для корректировки рациона ребенка родители могут обратиться к диетологу, который составит правильный план питания, подходящий для разных периодов болезни.
Язвенный колит и лечение препаратами
Основная задача в ходе терапевтического процесса — частично или полностью купировать воспаление и ослабить влияние на кишечник болезнетворных микроорганизмов. Для этого назначаются противовоспалительные лекарственные средства. Сложность процесса протекания неспецифического язвенного колита у детей зависит от симптомов и эффективности лечения.
Медикаментозная корректировка состояния пациента включает прием таких лекарств:
- Глюкокортикоидов (особенно эффективны при левосторонних формах колита);
- Антибиотиков (рекомендованы в моменты рецидива, в том числе при повышенных показателях температуры тела).
При отсутствии ожидаемых результатов в рамках лечения, а также в экстренных случаях детям с НЯК рекомендована операция. Большинство пациентов не нуждаются в радикальном вмешательстве хирургов, но, согласно статистике, примерно в 20-40 процентах случаев, по мере усугубления патогенных процессов, требуется удаление части кишки.
На что жалуется ребенок
Боль в области живота — характерный признак НЯК. Ребенок, помимо болевых ощущений, теряет аппетит и может жаловаться на чувство слабости. При дефиците питательных веществ в организме могут появиться другие внекишечные признаки, такие как головокружение, головная боль, небольшая температура.
У каждого третьего пациента с колитом выраженные воспалительные процессы приводят к перфорации. На фоне неправильной работы кишечника может появляться сепсис.
При отсутствии медикаментозного лечения и несоблюдении диеты не исключаются профузные кишечные кровотечения, трещины, свищи и другие осложнения, включая летальные исходы. Риски развития рака кишечника на фоне НЯК возрастают с каждым десятилетием жизни с соответствующим диагнозом в анамнезе.
Другие особенности симптоматики
В острой фазе неспецифического язвенного колита у ребенка нарушается стул. Во время испражнений фекалии могут содержать кровь.
Длительная диарея приводит к нарушению обмена веществ и вытекающей потере веса. У ребенка снижается аппетит, он отказывается от еды.
Выделяют ряд внекишечных симптомов, связанных с осложнениями НЯК:
- Дисфункция сердечной системы;
- Сосудистые поражения (тромбоз, тромбофлебит);
- Нарушения функций почек и печени.
Продолжительные воспалительные процессы в кишечнике у детей, оставленные без внимания взрослыми, приводят к сбоям в работе систем и органов всего организма, поэтому без квалифицированной медицинской помощи могут послужить причиной инвалидности.
Классификация заболевания
По степени распространенности поражения НЯК выделяют: дистальный, левосторонний, тотальный и субтотальный колит. Для оценки тяжести заболевания используется классификация по Трулав и Виттс:
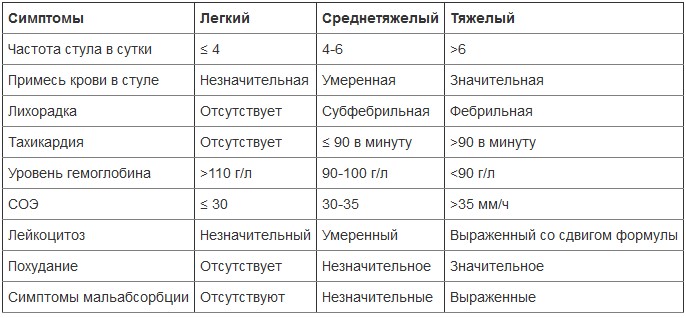
Классификация НЯК по характеру течения (виды):
- Рецидивирующий (чередование фаз ремиссии и обострения);
- Непрерывный (обострения в течение года происходят от 2 раз и чаще);
- Фульминантный (тяжелое течение и последующее развитие осложнений).
В зависимости от особенностей протекания патологии, помимо описанных клинических признаков воспаления, могут диагностироваться слизистые выделения из прямой кишки, вздутие живота, тенезмы, отеки ног, кожные высыпания, запоры и гематохезия.
Диагностические мероприятия при НЯК
При подозрениях на аутоиммунные заболевания проводятся лабораторные тесты. Анализы крови при НЯК показывают повышенное содержание лейкоцитов, а также заниженный уровень эритроцитов (типичный признак анемии из-за кишечных кровопотерь).
Образцы стула берутся с целью установить состав кала (вычисляется присутствие кровяных прожилок, слизи, а также устанавливаются потенциальные провокаторы состояния — паразиты и бактерии).
К дополнительным методам относят эндоскопию, колоноскопию и рентген с барием. При необходимости берется биопсия для дальнейшего исследования материала.
Прогнозы
Чтобы улучшить общее состояние, родителям важно учитывать социальные и эмоциональные изменения в жизни ребенка. Позитивные эмоции и поддержка близких оказывают не меньший положительный эффект, чем терапевтические методики.
Молниеносное (особо опасное развитие НЯК) происходит не более, чем в 10 процентах случаев. Более того, 10 процентов больных НЯК выздоравливают после одиночного приступа (однако вероятность рецидива в будущем сохраняется).
При поражениях больших областей толстого кишечника, по мере окончания 10-летнего периода с момента постановки диагноза, опасность развития рака увеличивается на 0,5-1 процент в год. Наибольшие риски онкологии — при тотальных случаях колита. Наиболее благоприятный прогноз делается пациентам с локальным язвенным проктитом.
Подписывайтесь на нас в социальных сетях
Поделиться ссылкой:
Источник
Использование лечебного питания в комплексной терапии хронических воспалительных заболеваний кишечника у детей
 Неспецифический язвенный колит и болезнь Крона остаются одной из наиболее серьезных проблем в современной гастроэнтерологии, так как характеризуются тяжелым течением, частыми рецидивами, развитием местных и системных осложнений, неблагоприятным прогнозом и инвалидизацией. У пациентов с хроническими воспалительными заболеваниями кишечника (ВЗК) также имеют место изменения нутритивного статуса, связанные с дефицитом белка, макро- и микроэлементов, энергетических субстратов. В педиатрической практике эта проблема особенно актуальна, так как питание является не только одним из важных факторов, определяющих адекватность течения воспалительного ответа и адаптационно-компенсаторных процессов, но также играет ключевую роль в процессах роста и развития больного ребенка.
Неспецифический язвенный колит и болезнь Крона остаются одной из наиболее серьезных проблем в современной гастроэнтерологии, так как характеризуются тяжелым течением, частыми рецидивами, развитием местных и системных осложнений, неблагоприятным прогнозом и инвалидизацией. У пациентов с хроническими воспалительными заболеваниями кишечника (ВЗК) также имеют место изменения нутритивного статуса, связанные с дефицитом белка, макро- и микроэлементов, энергетических субстратов. В педиатрической практике эта проблема особенно актуальна, так как питание является не только одним из важных факторов, определяющих адекватность течения воспалительного ответа и адаптационно-компенсаторных процессов, но также играет ключевую роль в процессах роста и развития больного ребенка.
Дети, страдающие этой тяжелой хронической патологией, как правило, имеют дефицит массы тела с уменьшением подкожно-жировой клетчатки и снижением тургора тканей (по нашим данным, отмечается у 40,3% детей с неспецифическим язвенным колитом и у 54,2% детей с болезнью Крона) [1], часто наблюдается отставание в росте, задержка полового созревания, снижение минерализации костной ткани.
Нарушения нутритивного статуса при хронических воспалительных заболеваниях кишечника обусловлены рядом причин:
недостаточным поступлением питательных веществ в организм ребенка в результате:
уменьшения всасывательной поверхности слизистой оболочки из-за воспалительного процесса или резекции части кишечника;
ферментативной недостаточности (синдром мальабсорбции, синдром «короткой кишки»);
отсутствия аппетита или отказа от приема пищи ввиду болей в животе, возникающих после еды, метеоризма, тошноты;
повышенными потерями питательных веществ (хроническая кровопотеря, обусловленная выделением крови с калом, экссудация кишечником белков плазмы крови);
увеличением энергозатрат в связи с развитием системного воспалительного процесса (повышение температуры тела, увеличение частоты пульса и дыхания, синтез белков «острой фазы»).
Кроме того, усилению катаболических процессов способствует гиперпродукция мононуклеарами крови провоспалительных цитокинов или длительная терапия кортикостероидами [5].
Коррекция нутритивных нарушений обеспечивается назначением адекватного лечебного питания, которое необходимо рассматривать как одно из основных направлений в составе комплексной терапии хронических воспалительных заболеваний кишечника у детей.
Лечебное питание должно строиться с учетом возраста ребенка, нозологии, фазы патологического процесса, характера функциональных и морфологических изменений кишечника, сочетанной патологии органов пищеварения.
Общепризнанной формулы диетического питания при ВЗК у взрослых пациентов и у детей не существует [3, 4]. Задача врача состоит в том, чтобы подобрать больному индивидуальную диету, которая не вызывала бы у него неприятных субъективных ощущений и способствовала бы сохранению длительной ремиссии. Рекомендуется ведение пищевого дневника родителями больного ребенка с учетом рациона и характера стула для своевременной диагностики непереносимости отдельных продуктов и диетической коррекции.
В условиях стационара при обострении неспецифического язвенного колита и болезни Крона у детей рекомендуется лечебный рацион на основе диеты № 4б.
Адекватное поступление нутриентов и энергии можно обеспечить путем энтерального и парентерального питания.
Возможность использования полного парентерального питания как первичного метода лечения и его способность уменьшить активность тяжело протекающего язвенного колита и болезни Крона у детей остается недостаточно изученной. Парентеральное питание применяется как дополнительное в случаях выраженной недостаточности питания или как полное при наличии таких осложнений, как кишечная непроходимость, токсическая дилятация толстой кишки, тяжелые нарушения всасывания [7].
В отличие от парентерального питания, проведение нутритивной поддержки с помощью энтерального питания является более физиологическим методом, так как способствует поддержанию функции желчеотделения и поджелудочной железы, служит стимулом для выработки гастроинтестинальных пептидов, способствует восстановлению всасывательной и моторно-эвакуаторной функций кишечника и сохранению защитного барьера, отделяющего патогенные микроорганизмы от системной микроциркуляции.
Энтеральное питание с использованием стандартных диет применяется в качестве самостоятельного метода лечения, а также в комбинации с лекарственной терапией. Последние исследования показали высокую эффективность энтерального питания, применение которого приводит не только к коррекции дистрофических нарушений и дефицитных состояний, но и обеспечивает индукцию ремиссии не менее эффективно, чем введение глюкокортикостероидов при лечении болезни Крона у детей [8, 9].
Выделяют три группы смесей для энтерального питания: элементные (смеси на основе аминокислот), полуэлементные (содержащие олигопептиды) и полимерные (высокомолекулярные смеси на основе цельного белка).
Новым перспективным направлением является лечебное питание с использованием так называемых иммуномодулирующих продуктов, примером которых является специально разработанная для пациентов с хроническими воспалительными заболеваниями кишечника смесь Modulen IBD (Nestle). Смесь обогащена естественным противовоспалительным фактором роста (TGF-бета2) — полипептидом, который участвует в обеспечении роста и дифференцировки эпителиальных клеток кишечника, а также в иммунной регуляции, подавляя синтез провоспалительных цитокинов. Этот полипептид обнаруживается как в женском, так и в коровьем молоке, но разрушается при обычных способах его обработки. Содержание TGF-бета2 в смеси составляет более 24 ppm. Белковый компонент продукта представлен казеинами; углеводный — полимерами глюкозы и сахарозой; жировой: смесью молочного жира, кукурузного масла и среднецепочечными триглицеридами. Продукт содержит адекватное количество витаминов, минеральных веществ. Смесь не содержит лактозу и глютен, может применяться у детей с 5-летнего возраста.
Высокая эффективность энтерального питания с использованием полимерной смеси Modulen IBD (Nestle) детям с болезнью Крона продемонстрирована в двух исследованиях.
В первом проспективном исследовании 29 пациентов с тяжелой и среднетяжелой формой болезни Крона получали смесь в качестве монотерапии и единственного источника питания на протяжении 8 недель. За исключением одного ребенка, все дети принимали индивидуально рассчитанный объем смеси (в среднем 2500 мл) перорально с хорошей переносимостью. Была достигнута положительная клиническая и биохимическая динамика (снижение С-реактивного белка), улучшение эндоскопической и гистологической картины со стороны слизистой оболочки кишечника, а также достоверное снижение уровня провоспалительных цитокинов (интерлейкина-1, интерлейкина-8, интерферона-альфа) в биоптатах подвздошной и толстой кишки, что позволило достигнуть длительной ремиссии у 75% детей [10].
Во втором открытом, проспективном, рандомизированном исследовании 19 пациентов с активной болезнью Крона получали полимерную диету Modulen IBD в течение 10 недель и 18 пациентов метилпреднизолон внутрь (1,6 мг/кг/день в течение четырех недель, с последующим снижением дозы). Было показано, что нутритивная терапия так же эффективна в индукции клинической ремиссии, как и короткий курс кортикостероидной терапии, и достоверно более эффективна для восстановления слизистой, что было подтверждено эндоскопически и гистологически через 10 недель от начала терапии [8].
С целью коррекции нутритивного статуса смесь лечебного питания может быть использована на фоне базисной терапии дополнительно к лечебному столу.
На базе нашего института мы имеем опыт применения смеси Modulen IBD в качестве дополнительного питания. Смесь назначалась в дозе 200-600 мл в сутки (в среднем, по 150 мл на второй завтрак и полдник) в течение 3-6 недель дополнительно к безмолочному диетическому столу (№ 4 по Певзнеру). Под наблюдением находилось 24 ребенка в возрасте от 2 до 17 лет (средний возраст 12,3 года). Десять пациентов с неспецифическим язвенным колитом и четырнадцать с болезнью Крона. Четверо детей были в послеоперационном периоде, оперативное вмешательство выполнялось в связи с развитием осложнения болезни Крона (стенозирование кишки). До назначения лечебного питания физическое развитие было нормальным лишь у 5 пациентов, остальные наблюдавшиеся имели дефицит массы тела (табл.).
При использовании Modulen IBD у 22 из 24 пациентов была отмечена хорошая переносимость продукта. Отрицательная реакция на применение смеси была у мальчика 14 лет с неспецифическим язвенным колитом на 5-6 день приема в виде появления примеси крови в кале, которая купировалась после ее отмены и назначения сорбентов. Еще у одной пациентки с болезнью Крона при употреблении смеси отмечено увеличение кратности стула с трех до пяти раз в день. Клинико-анамнестические данные у первого пациента позволяют связать реакцию с индивидуальной непереносимостью белка казеина. У всех детей, получавших смесь Modulen IBD полным курсом в составе комплексной терапии, отмечена положительная клиническая динамика в виде улучшения самочувствия, уменьшения выраженности астении, трофических нарушений, прибавки в массе от 500 г до 4 кг (в среднем 1,8 кг), уменьшения клинико-лабораторных показателей активности по основному заболеванию. Кроме того, имело место улучшение характера стула (снижение кратности до 1-2 раз в день, густая консистенция). Дополнительно следует отметить хорошие вкусовые качества смеси, что обеспечивает повышение аппетита, положительный эмоциональный настрой ребенка и заменяет в питании молоко детям, чувствующим себя ущербными на постоянной безмолочной диете.
Эффективность лечебного питания при болезни Крона можно продемонстрировать следующим клиническим наблюдением.
Пациент М, 16 лет, наблюдается в НИИ детской гастроэнтерологии с 11-летнего возраста, когда впервые у него была диагностирована болезнь Крона с множественной локализацией (в подвздошной кишке, сигмовидной кишке и аноректальной зоне). Пациент длительно получал терапию месалазином внутрь и ректально, топические стероиды (будесонид). В последующем течение заболевания приняло торпидный характер, по данным рентгенологического обследования выявлен стеноз подвздошной кишки с нарастанием по протяженности в течение года, в связи с чем произведено плановое оперативное лечение. Было удалено около 70 см подвздошной кишки с тремя участками стеноза, язвенным поражением, произведена резекция слепой кишки. После оперативного лечения длительно сохранялись явления сопутствующего пиелонефрита.
Мальчик получал постоянную поддерживающую терапию месалазином. В ноябре 2008 года при прохождении планового обследования в институте в статусе было отмечено: сниженная масса тела (рис.), нарушение осанки, выраженная сухость кожи, остаточные проявления герпетических высыпаний в области губ, хейлит. Живот безболезненный, мягкий. Аппетит сниженный, избирательный. Стул до трех раз в день, кашицеобразный, без видимых патологических примесей. Клинический анализ крови без воспалительных изменений. По данным колоноскопии воспалительных изменений в толстой кишке не было выявлено, анальные трещины эпителизированы. При проведении видеокапсульной эндоскопии выявлен тотальный эрозивно-язвенный процесс тонкой кишки, желудка, двенадцатиперстной кишки. В связи с отказом родителей от назначения стероидов ребенку было назначено дополнительное лечебное питание специализированной смесью Modulen IBD по 150-200 мл ´ 3 раза в день в течение 6 недель.
При повторном обследовании, несмотря на то, что по данным видеокапсульной эндоскопии положительной динамики на фоне лечения не было получено (сохранялся распространенный эрозивно-язвенный процесс), была отмечена положительная динамика в виде улучшения аппетита и самочувствия, купирования дистрофических изменений кожи, прибавки в массе 4,3 кг, восстановления индекса массы тела (19 кг/м2). Использование дополнительного лечебного питания специализированной смесью у данного больного позволило эффективно корректировать нутритивный статус пациента, даже в случае множественной локализации болезни Крона.
Смесь Modulen IBD может быть использована у детей с хроническими воспалительными заболеваниями кишечника в активной фазе заболевания, а также в послеоперационном периоде, за исключением пациентов, имеющих непереносимость казеина.
Таким образом, на современном этапе лечебное питание рассматривается как один из методов патогенетической терапии хронических воспалительных заболеваний кишечника. Диетотерапия должна строиться индивидуально с учетом возраста ребенка, нозологии, фазы патологического процесса, характера функциональных и морфологических изменений кишечника, сочетанной патологии органов пищеварения. Перспективным направлением представляется применение энтерального (зондового и сипингового) питания с использованием специализированных смесей, как в качестве дополнительной терапии к медикаментозному лечению с целью коррекции белково-энергетической недостаточности, так и в качестве эффективной монотерапии с целью индукции и поддержания ремиссии.
Литература
Богомолов А. Р. Клинические особенности заболеваний, протекающих с кровью в стуле у детей: Автореф. дис. … канд. мед. наук. Нижний Новгород, 2002. 22 с.
Bistrian B. Role of the systemic inflammatory response in the development of protein-energy malnutrition in Inflammatory bowel disease // Inflammatory Bowel Diseases: Nestle Nutrition Workshop Series Clinical & Performance Programme. 1999. V. 2, p. 1-6.
Адлер Г. Болезнь Крона и язвенный колит. Перевод с нем. М.: Гоэтар-Мед, 2001. С. 296-303; 427-429.
Беренс Р., Будерус Ш., Келлер К.-М., фон дер Остен-Сакен И. Болезнь Крона и язвенный колит у детей и подростков. Практическое руководство. Dr. Falk Pharma GmbH. 2005. С. 46.
Каншина О. А., Каншин Н. Н. Неспецифический язвенный колит у детей (и врослых) М.: Биоинформсервис, 2002. 212 с.
Рославцева Е. А., Боровик Т. Э., Мазанкова Л. Н. Современные представления о лечебном питании при болезни Крона в детском возрасте // Вопросы детской диетологии. 2003. т. 1, № 2, с. 24-27.
Халиф И. Л., Лоранская И. Д. Воспалительные заболевания кишечника (неспецифический язвенный колит и болезнь Крона) клиника, диагностика и лечение. М.: Миклош, 2004. 88 с.
Borelli O. et аl. Polymeric Diet Alone Versus Corticosteroids in the Treatment of Active Pediatric Crohn’s Disease: A Randomized Controlled Open-Label Trial // Clinical Gastroenterologi and hepatologi. 2006. V. 4. № 6. P. 1-10.
Griffits A. Enteral nutrition in children // Inflammatory bowel disease. Nestle Nutrition Workshop Series, Clinical & Performance Programme. 1999. № 2. P. 31-33.
Fell J. M., Paintin M., Arnaud-Battandier F. et al. Mucosal healing and a fall in mucosal pro-inflammatory cytokine mRNA induced by a specific oral poly meric diet in paediatric Crohn’s disease // Aliment. Pharmacol. Ther. 2000. V. 14 (3). P. 281-289.
О. А. Тутина
Э. Н. Федулова, кандидат медицинских наук
Л. В. Бейер, доктор медицинских наук
О. В. Федорова, кандидат медицинских наук
НИИ детской гастроэнтерологии Росмедтехнологий, Нижний Новгород
Контактная информация об авторах для переписки: tutina_oa@mail.ru
Характеристика группы пациентов, получавших смесь лечебного питания Modulen IBD
Рис. Динамика клинических и эндоскопических параметров у пациента с болезнью Крона
Источник