Кортикостероиды для лечения колита
Содержание статьи
Роль системных и топических кортикостероидов в терапии язвенного колита
В статье рассмотрена роль системных и топических кортикостероидов в терапии язвенного колита
Язвенный колит (ЯК) представляет собой хроническое идиопатическое воспалительное заболевание с повреждением слизистой оболочки толстой кишки. При ЯК поражается только толстая кишка (за исключением ретроградного илеита), в процесс обязательно вовлекается прямая кишка, воспаление чаще всего ограничивается слизистой оболочкой (за исключением фульминантного колита) и носит диффузный характер. ЯК характеризуется периодами активного проявления симптомов заболевания, которые перемежаются периодами клинической ремиссии [1]. В 2012 г. статистический анализ показал, что в мире распространенность ЯК достигла 249 на 100 тыс. человек в Северной Америке и 505 на 100 тыс. человек в Европе; самые высокие годовые показатели заболеваемости ЯК были 19,2 на 100 тыс. человеко-лет в Северной Америке и 24,3 на 100 тыс. человеко-лет в Европе [2]. Самый высокий уровень заболеваемости, по-видимому, отмечается в возрасте 20–30 лет, хотя есть некоторые доказательства второго пика заболеваемости в более позднем возрасте [2]. Однако наличие второго пика заболеваемости признается не всеми специалистами, занимающимися воспалительными заболеваниями кишечника (ВЗК).
Эндоскопическое исследование толстой кишки у больных ЯК выявляет ряд характерных повреждений слизистой оболочки толстой кишки (СОТК): отсутствие сосудистого рисунка, гиперемию, зернистость, контактную кровоточивость, наличие эрозий и язв [1, 3]. В настоящее время заживление СОТК при ЯК рассматривается как одна из ключевых конечных точек в клинических исследованиях, а достижение заживления СОТК в клинической практике – как реальная возможность изменить течение ЯК и сохранить функции кишечника. В исследованиях последних лет показано, что заживление СО как при ЯК, так и при болезни Крона (БК) достоверно связано с большей продолжительностью клинической ремиссии заболевания, более низкой частотой рецидивов, более низким риском развития колоректального рака и более высоким качеством жизни [4, 5], а также существенно меньшей частотой кол-эктомий [6].
Существующие руководства по лечению взрослых больных ЯК в США [7], Европейском союзе [8] и Российской Федерации [9] рекомендуют в качестве первой линии терапии для индукции ремиссии у пациентов с легкой и среднетяжелой формами ЯК препараты 5-аминосалициловой кислоты (5-АСК). Такое лечение считается наиболее эффективным при комбинации системных и пероральных препаратов 5-АСК [7–9]. В случае неэффективности 5-АСК препаратами второй линии являются глюкокортикостероиды (ГКС) [7–9]. Однако ГКС I поколения, такие как преднизолон, имеют ряд побочных эффектов: повышенный риск развития инфекционных осложнений, остеопороза, синдрома Иценко – Кушинга, развитие стероидного диабета, симптоматической гипертензии и даже повышенный риск смертности по сравнению с таковым в общей популяции [7, 10–12].
В настоящее время для лечения ВЗК применяется несколько глюкокортикоидов топического действия для приема внутрь и для ректального введения: будесонид, тиксокортола пиволат, беклометазон, флютиказон [13]. В России с 2004 г. зарегистрирован и успешно применяется препарат Буденофальк (компания Dr. Falk, Германия) в форме капсул для приема внутрь. Одна капсула Буденофалька содержит 3 мг будесонида. При ряде заболеваний, например при бронхиальной астме и сезонном аллергическом рините, будесонид так же эффективен, как системные ГКС, отличаясь при этом лучшей переносимостью и меньшим влиянием на гипоталамо-гипофизарно-адреналовую систему. Это послужило основанием для применения будесонида при БК. Будесонид является первым топическим кортикостероидом, имеющим сродство к глюкокортикоидным рецепторам приблизительно в 8,5, 15 и 195 раз больше, чем у дексаметазона [14], преднизолона [15] и гидрокортизона [15] соответственно. Кроме того, будесонид почти не всасывается из кишечника, характеризуется низкой системной биодоступностью (не более 10% по сравнению с таковой преднизолона и гидрокортизона) и быстрым пресистемным метаболизмом. Последнее обеспечивает отсутствие токсичных метаболитов в крови после первого прохождения препарата через печень. Однако наиболее высокая внутрипросветная концентрация действующего вещества и, соответственно, наибольшая эффективность Буденофалька достигаются, начиная с терминального отдела подвздошной кишки и до поперечной ободочной кишки.
ЯК – это хроническое заболевание, поражающее только СОТК, сопровождающееся ее воспалением, отеком и образованием язвенных дефектов. Воспаление всегда начинается с прямой кишки, непрерывно распространяясь выше вплоть до поражения СО всех отделов толстой кишки. Таблетированный мультиматричный (ММХ) будесонид является представителем II поколения кортикостероидов, созданным для доставки активного вещества на протяжении всей толстой кишки. В фармакокинетических исследованиях среднее относительное всасывание будесонида в месте между восходящей кишкой и нисходящей/сигмовидной кишкой составило 95,9% (рис. 1) [16]. В 2-х похожих по дизайну исследованиях 3-й фазы (CORE I и II) однократный ежедневный прием будесонида ММХ 9 мг оказался эффективным и хорошо переносимым для индукции ремиссии ЯК легкой и средней степени тяжести. Частота клинической и эндоскопической ремиссии составила 17,9% (CORE I) и 17,4% (CORE II) для будесонида ММХ 9 мг по сравнению с плацебо 7,4% и 4,5% соответственно (p<0,05, будесонид ММХ 9 мг по сравнению с плацебо в обоих исследованиях), 12,1% с месалазином 2,4 г и 12,6% с будесонидом 9 мг, высвобождаемым в подвздошной кишке. По данным исследования поддерживающей терапии будесонидом в течение 12 мес., будесонид ММХ 6 мг может удлинять время до рецидива заболевания: среднее время составило 1 год для будесонида ММХ 6 мг по сравнению с 181 днем (р=0,02) для плацебо; однако необходимы дальнейшие исследования. В исследованиях CORE будесонид ММХ проявил хороший профиль безопасности; большинство нежелательных явлений (НЯ) были легкими или умеренными по своей интенсивности, серьезные НЯ были очень редкими. Более того, частота побочных реакций, возможно, связанных с глюкокортикоидами, была сравнима среди групп лечения. Долгосрочная безопасность (12 мес.) будесонида ММХ была сравнима с таковой плацебо. Эти данные подтверждают возможность включения ММХ будесонида в алгоритм лечения ЯК [17–20].
Будесонид ММХ для лечения и индукции ремиссии ЯК
Эффективность и безопасность будесонида ММХ для индукции ремиссии пациентов с легкой и умеренной активностью ЯК (индекс активности заболевания 4–10) изучались в похожих по дизайну рандомизированных исследованиях CORE I и CORE II [17–20]. В CORE I сравнивали будесонид ММХ 9 мг и 6 мг с месалазином 2,4 г и плацебо, тогда как в CORE II сравнивались те же дозы будесонида ММХ с будесонидом 9 мг, высвобождающимся в подвздошной кишке, и плацебо. В обоих исследованиях терапия проводилась 8 нед., и первичными точками были клиническая и эндоскопическая ремиссия на 8-й нед. лечения. Ремиссия определялась как индекс активности ЯК ≤ 1 со значением 0 для ректального кровотечения и частоты стула, отсутствие ранимости СО при колоноскопии, и снижение ≥ 1 эндоскопического индекса от исходного значения. В обоих исследованиях клиническая и эндоскопическая ремиссия была достигнута у значительной части пациентов, получавших будесонид ММХ 9 мг (по сравнению с плацебо). В исследовании CORE I ремиссия на 8-й нед. была достигнута у 17,9% пациентов, получавших будесонид ММХ 9 мг, у 7,4% (р=0,01) в группе плацебо и у 12,1% в группе, получавшей месалазин. В исследовании CORE II частота ремиссии к 8-й нед. составила 17,4% у пациентов, получавших будесонид ММХ 9 мг, по сравнению с 4,5% (p=0,005) и 12,6% (p=0,048) в группах, получавших плацебо и будесонид, высвобождающийся в подвздошной кишке, соответственно. Кроме этого, анализ подгруппы в исследовании CORE II показал, что при приеме будесонида ММХ 9 мг существенно большая часть пациентов с левосторонним ЯК достигла клинической и эндоскопической ремиссии, чем при приеме плацебо (17,7% по сравнению с 5,8% соответственно; p=0,03); часть пациентов с распространенным заболеванием, которые достигли клинической и эндоскопической ремиссии, также была больше при использовании будесонида ММХ 9 мг, чем при использовании плацебо (13,8% по сравнению с 0% соответственно), но это различие не было статистически значимым (p=0,10). В исследовании CORE I анализ подгрупп по тяжести заболевания показал, что у пациентов с легким течением ЯК (индекс активности ЯК 4 или 5), которые получали будесонид ММХ 9 мг или плацебо, клиническое улучшение (определялось как снижение ≥ 3 баллов индекса активности ЯК) было достигнуто у 44,4% и 25,0% пациентов соответственно; у пациентов с умеренной активностью заболевания (индекс ЯК ≥ 6 и ≤10) показатели клинического улучшения составили 39,7% и 30,1% соответственно. Более того, частота заживления СО была больше при применении будесонида MMX 9 мг, чем при применении плацебо, у пациентов с проктосигмоидитом (32,4% по сравнению с 19,5% соответственно; p=0,20) и левосторонним ЯК (40,6% по сравнению с 26,5% соответственно; p=0,22). Похожее различие в пользу будесонида ММХ 9 мг наблюдалось у пациентов с распространенным ЯК (16,1% по сравнению с 10,0% при применении плацебо), но это различие также не было статистически значимым (p=0,39). В анализе исследований CORE I и CORE II пациенты, получающие будесонид ММХ 9 мг, достигали клинической и эндоскопической ремиссии в 3 раза чаще, чем при получении плацебо [ОШ 3,3 (95% ДИ 1,7–6,4)]. Будесонид ММХ 9 мг был статистически значимо более эффективен по сравнению с плацебо у нескольких групп пациентов: мужского и женского пола ≤ 60 лет; ранее принимавших месалазин; не получавших месалазин ранее; с легким течением ЯК на исходном уровне; со средней тяжестью ЯК исходно; с проктосигмоидитом; с левосторонним ЯК; с длительностью ЯК ≥ 1 года и ≤5 лет; с длительностью ЯК > 5 лет.
Будесонид ММХ 9 мг для поддержания ремиссии ЯК
Эффективность будесонида ММХ 9 мг для поддержания ремиссии была изучена у пациентов, которые достигли клинической и эндоскопической ремиссии в исследованиях CORE I и CORE II, у пациентов в исследованиях CORE I и II, которые получали дополнительно 8 нед. лечения (будесонид ММХ 9 мг), и открытом исследовании, в котором пациенты были рандомизированы на группы, получавшие будесонид ММХ 6 мг или плацебо в течение 12 мес.; первичная точка эффективности – клиническая ремиссия, которая оценивалась через 1, 3, 6, 9 и 12 мес. Среднее время до рецидива заболевания (определялось как ректальное кровотечение, частота стула более чем 1–2 р./сут или оба этих фактора) составило 181 день в группе плацебо, но не было достигнуто в группе будесонида ММХ (p=0,02); к 12 мес. вероятность рецидива составила 59,7% и 40,9% соответственно. Однако процентное соотношение пациентов, у которых ремиссия поддерживалась в течение 12 мес., не различалось существенно между группами, что, возможно, связано со статистическими недостатками исследования.
Следовательно, польза будесонида ММХ в поддержании ремиссии в настоящее время недостаточно ясна, и необходимо проведение дальнейших исследований [21].
Побочные эффекты
В целом у молекулы будесонида более благоприятный профиль безопасности, чем у I поколения пероральных кортикостероидов, таких как преднизон или преднизолон. Например, в двойном слепом исследовании в течение 10 нед. 176 пациентов с БК, которые получали преднизолон по схеме снижения или будесонид, высвобождающийся в подвздошной кишке, в течение 10 нед., частота побочных явлений, связанных с глюкокортикоидами, была значительно ниже при применении будесонида, чем преднизолона (33% по сравнению с 55% соответственно; p=0,003). Кроме этого, подавление гипоталамо-гипофизарно-надпочечниковой системы, оцениваемое с помощью измерения средней концентрации кортизола в плазме, было существенно выше при применении преднизолона, чем будесонида, высвобождавшегося в подвздошной кишке, через 4 нед. (р<0,001) и 8 нед. (р=0,02). Благоприятный профиль НЯ будесонида ММХ у пациентов с ЯК был показан в исследованиях CORE I и II.Частота НЯ у пациентов, получающих будесонид ММХ 9 мг или 6 мг, составила 57,5% и 58,7% соответственно в исследовании CORE I, 55,5% и 62,5% соответственно – в CORE II. В обоих исследованиях большинство НЯ было легкими или умеренными по интенсивности, частота серьезных НЯ была ниже и схожей во всех группах лечения. Наиболее распространенными НЯ у пациентов, получавших будесонид ММХ, были головная боль, тошнота. В исследованиях CORE I и II частота НЯ, возможно, связанных с ГКС (акне, задержка жидкости, гиперемия, гирсутизм, инсомния, изменение настроения, «лунное» лицо, нарушение сна, образование стрий), была сравнима с таковой для будесонида ММХ 9 мг (10,2%), 6 мг (7,5 %) и плацебо (10,5%). Самыми распространенными НЯ, возможно, связанными с ГКС, при применении будесонида ММХ 9 мг по сравнению с плацебо были изменения настроения (3,5% и 4,3% соответственно) и нарушение сна (2,7% и 4,7% соответственно). В исследовании будесонида ММХ 6 мг в течение 1 года профиль безопасности был сравним с таковым плацебо [22].
Клиническое наблюдение
Больной Б., 22 года. Болен с 2013 г., диагноз «язвенный колит» поставлен при колоноскопии в ГНЦ колопроктологии и подтвержден гистологически в 2013 г. Принимал постоянно месалазин 3 г/сут. Амбулаторно проведена колоноскопия 24.11.2014 г.: язвенный колит, тотальное поражение, минимальная активность. С января 2016 г. отменил прием препаратов 5-АСК. В феврале 2016 г. отметил появление примеси крови в стуле. Возобновил прием месалазина 3 г/сут со слабоположительным эффектом, кровь в стуле сохранялась.
Однако с середины марта 2016 г. состояние ухудшилось, кроме примеси крови в стуле отмечались диарея до 17 р./сут, периодическое повышение температуры тела до 38° С в вечернее время. При колонофиброскопии от 15.03.2016 г. колоноскоп проведен в дистальный отдел восходящей части толстой кишки, заключение: эндоскопическая картина ЯК (тотальное поражение), тяжелая степень активности (рис. 2). При ЭГДС – хронический гастродуоденит с признаками выраженного обострения процесса, дуоденогастральный рефлюкс, недостаточность кардии, Нр+. Самостоятельно увеличил дозу месалазина до 4 г/сут, микроклизмы месалазина 2 г/сут на ночь со слабоположительным эффектом в виде урежения стула до 12 р./сут, примесь крови сохранялась.
![Рис. 1. Сцинтиграфия здорового добровольца. Будесонид MMX меченый [153Sm] в толстой кишке. Изображение получено через 7 ч после приема препарата (Brunner et al., 2006) Рис. 1. Сцинтиграфия здорового добровольца. Будесонид MMX меченый [153Sm] в толстой кишке. Изображение получено через 7 ч после приема препарата (Brunner et al., 2006)](https://www.rmj.ru/upload/medialibrary/fdc/fdce054cd022b9f2e7afc1c307ee002c.png)
18.03.2016 г. поступил на стационарное лечение в ГБУЗ МКНЦ ДЗМ. В общем анализе крови от 18.03.2016 г. отмечались лейкоцитоз (9,6 × 109) с палочкоядерным сдвигом (28%), повышение СОЭ до 26 мм/ч. В биохимическом анализе крови от 18.03.2016 г. отмечались повышение СРБ до 133,37 мг/л, латентный дефицит железа – 5,4 мкмоль/л.
При УЗИ органов брюшной полости 18.03.2016 г.: стенка левых отделов отечная, гипоэхогенная, утолщена до 7–8 мм, гаустрация сглажена, дифференциация слоев прослеживается четко не везде, в просвете – жидкость и изоэхогенное содержимое, в толще стенки – гиперэхогенные включения, что может соответствовать наличию язвенных дефектов; по ходу нисходящего отдела и сигмовидной кишки воспалительная инфильтрация параколической клетчатки с включением л/узлов размером до 11×7 мм; свободная жидкость в правой подвздошной области в небольшом количестве; заключение: эхопризнаки язвенного колита, левостороннее поражение, воспалительная инфильтрация параколической клетчатки по ходу левых отделов ободочной кишки с лимфаденопатией, небольшое количество свободной жидкости в правой подвздошной области (рис. 3). Кальпротектин кала от 19.03.2016 г. – 840 мкг/г.
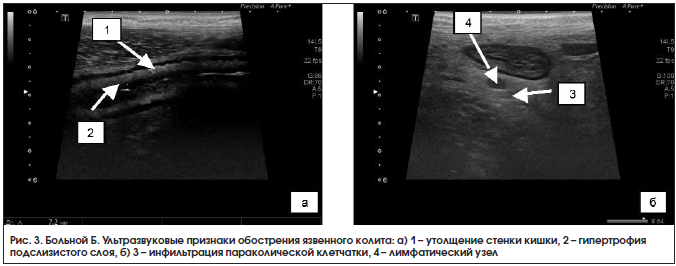
Установлен диагноз: язвенный колит, тотальное поражение, хроническое рецидивирующее течение, средней степени тяжести, умеренной активности. Латентный дефицит железа.
С учетом отсутствия у больного эффекта от терапии препаратами 5-АСК и категорического отказа от проведения терапии системными ГКС больному назначены Кортимент (топические ГКС) 9 мг/сут, месалазин 5 г/сут, микроклизмы с гидрокортизоном 125 мг 2 р./сут, метронидазол 500 мг 3 р./сут в/в, гидроксид железа 100 мг/сут № 3; цефтриаксон 2,0 г/сут в/в капельно.
На фоне терапии через 10 дней у больного отмечалось улучшение состояния в виде урежения стула до 2 р./сут, без примеси слизи и крови.
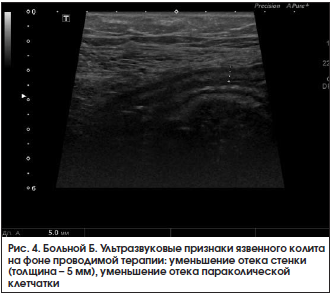
При контрольном УЗИ кишечника 28.03.2016 г.: по сравнению с предыдущим исследованием от 18.03.2016 г. отмечается положительная динамика. Тонкая кишка: петли не расширены, прослеживается ритмичная перистальтика, содержимое – средней эхогенности. Осмотрена ободочная кишка. В проекции слепой кишки, восходящего и поперечного отдела стенки не утолщены (2 мм), дифференциация слоев четкая. В проекции нисходящего отдела и сигмовидной кишки стенки толщиной 2,5–2,7 мм, слоистость стенки сохранена, более выражен подслизистый слой, в толще стенки сохраняются гиперэхогенные включения до 1,5 мм (вероятно, язвы). Клетчатка вокруг умеренно повышенной эхогенности с включением л/узлов размером до 8×3 мм. В правой подвздошной области межпетельно незначительное количество свободной жидкости. Заключение: эхопризнаки язвенного колита, левостороннее поражение, обострение. Мезентериальная лимфаденопатия (рис. 4). В общем анализе крови от 28.03.2016 г. сохраняется повышение СОЭ до 33 мм/ч. В биохимическом анализе крови от 28.03.2016 г. – нормализация уровня СРБ до 3,25 мг/л.
Заключение
Лекарственная формула будесонид ММХ доставляет лекарственное вещество в толстую кишку на всем ее протяжении [23], в то время как другие пероральные формы будесонида с контролируемым высвобождением работают только в дистальной части подвздошной кишки и в восходящей кишке – участках, которые наиболее часто поражаются воспалительным процессом при БК [24].
Будесонид ММХ является эффективным и хорошо переносится при применении с целью индукции ремиссии у пациентов с ЯК легкой и средней тяжести. Имеющиеся в настоящее время данные говорят о том, что этот препарат может быть эффективным и хорошо переноситься для поддержания длительной ремиссии (более 1 года) у пациентов с ЯК [17, 18]. Долгосрочная безопасность ММХ будесонида у пациентов с ЯК сравнима с таковой плацебо, эти данные представлены только в одном исследовании, которое длилось 12 мес. [19]. Однако в нескольких исследованиях изучали применение пероральных форм будесонида в качестве поддерживающей терапии у пациентов с БК, и это подтверждает долгосрочную (до 1 года) безопасность будесонида при поддержании ремиссии ВЗК [25–32]. Применение будесонида ММХ также может быть полезным в фармакоэкономическом плане в связи с возможным повышением приверженности терапии благодаря однократному приему препарата и снижению риска побочных явлений по сравнению с таковым при приеме традиционных пероральных кортикостероидов. Однако необходимо дальнейшее изучение этого препарата у пациентов с ВЗК.
Источник
Кортикостероиды для лечения колита —
Болезни желудочно-кишечного тракта
Использование кортикостероидов в лечении воспалительных болезней кишечника
Родовое название Название торговой марки
Некоторые из этих препаратов выпускаются в виде таблеток. Если заболевание поражает только нижнюю часть толстой кишки, кортикостероид может применяться в виде клизмы. В случае заболеваний, которые поражают прямую кишку, могут использоваться суппозитории и кремы местного действия. При острых заболеваниях кортикостероиды используются внутривенно.
Эти медикаменты уменьшают воспаление.
Почему применяют эти препараты
Кортикостероиды используются в лечении неспецифического язвенного колита и болезни Крона (воспалительных болезней кишечника или ВБК).
Неспецифический язвенный колит
Оральные или внутривенные кортикостероиды могут применяться в лечении:
Кортикостероидные препараты уменьшают или останавливают проявления симптомов неспецифического язвенного колита и болезни Крона. Эти медикаменты используются для того, чтобы спровоцировать длительную ремиссию болезни. После этого врач назначает меньшую дозу более слабого препарата.
Кортикостероиды назначают только тем людям, которые не поддаются лечению с использованием других препаратов (меньше, чем половина людей, которые болеют ВБК). У многих из таких людей начинается ремиссия заболевания после применения этих препаратов. Для того чтобы удерживать болезни в состоянии ремиссии, некоторым людям с ВБК необходимо принимать небольшие дозы кортикостероидов.
Стероидные клизмы могут быть достаточно эффективными в лечении воспаления нижней части толстой и прямой кишки.
Основные побочные эффекты кортикостероидов это:
При длительном применении могут возникать другие побочные эффекты:
О чем следует помнить
Кортикостероиды не советуют применять длительный период из-за возможных побочных эффектов. После прекращения приема этих препаратов симптомы ВБК могут возобновиться. Параллельно с кортикостероидами врач может назначить аминосалицилаты и иммуномодуляторы. Эти медикаменты могут предотвратить проявление симптомов после прекращения приема кортикостероидов.
Люди, которые принимают кортикостероиды в течение 2-3 месяцев, должны также принимать кальций и витамин Д или другие медикаменты, такие, как бисфосфонаты, для того, чтобы предотвратить развитие остеопороза. Врач также может назначить анализ на плотность, который может определить это заболевание.
Недлительный прием кортикостероидных препаратов детьми, в общем, считается безопасным. Длительно использование этих препаратов повышает не только риск задержки развития, но и появления побочных эффектов. Но негативное влияние ВБК на организм ребенка является более опасным, чем возможные побочные эффекты стероидов, которые контролируют заболевание. Применение кортикостероидных препаратов для лечения проявления симптомов во время беременности является безопасным.
Стероидные клизмы нового поколения могут использоваться для длительного лечения ВБК, поскольку клизма вызывает меньшее количество побочных эффектов, которые поражают весь организм.
Использованные источники: www.eurolab.ua
Лечение неспецифического язвенного колита — группы препаратов: действие и способ применения, ограничения
Неспецифический язвенный колит (сокращенно называют НЯК) является хроническим, рецидивирующим воспалительным расстройством толстой кишки, этиология которого до сих пор выясняется.
Стратегии терапии заболевания в первую очередь направлены на борьбу с воспалением в период обострения, а также на поддержание организма пациента во время ремиссии.
Разработка новых биологических методов терапии изнурительной болезни продолжается, ученые разрабатывают медикаменты для лечения неспецифического язвенного колита, которые способны за максимально короткий срок избавить пациентов от симптомов НЯКа.
Медикаментозная терапия
Несмотря на усилия со стороны ученых и проведение клинических исследований, существует небольшое количество медикаментов способных справиться с течением неспецифического язвенного колита кишечника.
Лекарства, которыми лечат НЯК, назначают для преодоления рецидивов, контролирования воспаления, снижения риска развития рака.
Назначение препаратов зависит от течения недуга. НЯК может быть легким, умеренным или тяжелым. Дозировка медикаментов тоже меняется в зависимости от тяжести.
Фактически, успешность лечения заболевания зависит от количества лекарственного средства. Поэтому было разработано множество различных рецептур для определения действия препарата на недуг.
Пациентам при язвенном колите приходится принимать большое количество таблеток для достижения целевой эффективности использования лекарств. После уменьшения проявлений курс терапии корректируется, это также важно, ведь используемые при НЯК препараты негативно влияют на другие системы организма.
Текущие медицинские исследования проводятся для разработки новых более эффективных лекарств, они направлены на улучшение имеющихся медикаментов для получения оптимальных терапевтических результатов с максимальной безопасностью и минимальными побочными эффектами для пациентов, страдающих от неспецифического язвенного колита в кишке.
Аминосалицилаты или медикаменты 5-АСК
Использование лекарственных средств этой группы позволяет добиться стойкой ремиссии в 80% случаев НЯК.
Аминосалицилаты представляют собой наиболее распространенную линию лечения для больных с легким и умеренным течением язвенного колита.
Лекарства 5-АСК считаются эффективными, как для лечения острого вида заболевания, так и для поддержания в период ремиссии.
- Первым препаратом, принадлежащим к этому классу является Сульфасалазин, ранее был разработан для терапии ревматоидного артрита. Медикамент в толстой кишке метаболизируется бактериогенной азозоредуктазой в сульфапиридин и 5-аминосалициловую кислоту (5-ASA), являющейся фактическим биологически активным и эффективным агентом. Сульфасалазин можно считать первым препаратом, которые на протяжении многих лет с успехом используется в индуцировании ремиссии у больных с мягким и умеренным колитом. Для получения надлежащего лекарственного эффекта следует пить по 2–4 пилюли в день. Лечить воспалительное заболевание также можно суппозиториями Сульфасалазин. Свечи вводят в прямую кишку 2 р/день.
- Асакол. Лекарственное средство противопоказано принимать при язвенной болезни желудка, печеночной или почечной недостаточности, в последнем триместре беременности. Асакол при остром течении воспалительного заболевания принимают по 400–800 мг 3р./сутки, длительность употребления 2–3 месяца. Для профилактики заболевания рекомендуется принимать таблетки по 400–500 мг 3р./день.
В дополнение к оральным препаратам 5-АСК также можно использовать свечи (об этом немного ниже). Лечение язвенного колита ректальными средствами позволяют быстрее избавиться от заболевания.
Кортикостероиды
Глюкокортикостероиды предназначены для пациентов, испытавших рецидив заболевания.
Лекарства данной группы также назначают пострадавшим, не реагирующим на 5-АСК или при умеренных и тяжелых течениях язвенного колита неспецифического характера.
Их использование ограничено индукцией ремиссии, поскольку кортикостероиды не играют никакой роли в поддерживающей терапии.
Препараты используют местно, устно или парентерально. Способ применения зависит от тяжести заболевания.
Использованные источники: proktolog-info.ru
Применение глюкокортикостероидов для лечения неспецифического язвенного колита
Наиболее эффективными противовоспалительными средствами при неспецифическом язвенном колите остаются глюкокортикостероиды, которые блокируют освобождение арахидоновой кислоты, предотвращают образование медиаторов воспаления, оказывают иммуномодулирующее действие, влияют на тканевой фибринолиз, что приводит к уменьшению воспаления и кровоточивости слизистой оболочки.
Показания к назначению глюкокортикостероидов:
- левосторонние и тотальные формы язвенного колита с тяжелым течением, III степенью активности;
- острые тяжелые и среднетяжелые формы заболевания с наличием внекишечных проявлений;
- отсутствие эффекта от других методов лечения.
Доза преднизолона составляет 0,5-1 мг/кг, а при острых тяжелых формах 1 — 1,5 мг/кг вдень внутрь или в свечах (1 свеча содержит 5 мг преднизолона). Указанную дозу рекомендуется принимать до получения терапевтического эффекта (3-4, реже до 6 нед), затем ее снижают по 10 мг каждые 10 дн до 30 мг/сут, а в последующем снижение дозы преднизолона осуществляется постепенно на 2,5 мг каждые 7-10 дн. Поддерживающую дозу в 5 мг больной может принимать ежедневно или, что более оправдано, 10 мг через день.
Общий курс лечения преднизолоном составляет 6-9 мес. Можно использовать и гидрокортизон в дозе 250-500 мг/сут внутримышечно или 125 мг ректально. До полной отмены гормонов больные принимают сульфасалазин или салофальк.
Ред. проф. И.Н. Броновец
«Применение глюкокортикостероидов для лечения неспецифического язвенного колита» статья из раздела Гастроэнтерология
Использованные источники: www.primamunc.ru
Какие препараты принимать при язвенном колите | Как лечить язвенный колит лекарствами
Язвенный колит устраняется, когда больной включает в состав лечения медикаментозные средства, контролирующие диарею и изменения в пищеварении. У некоторых больных в течение продолжительного времени наблюдаются острые симптомы данной болезни, так иногда лечение требует хирургического вмешательства и дополнительных медикаментов.
Какие препараты принимать при язвенном колите?
Существует две категории данных средств для лечения язвенного колита:салазопрепараты и глюкокортикоиды. Каждая из них объединяется общностью фармакологических свойств входящих в их состав лекарственных агентов. Оговорим только, что сейчас намечается тенденция к замене салазопрепаратов на 5-аминосалициловую кислоту, которая является одной из их составляющих [Dorner W., 1986].
Как и при других кишечных заболеваниях, диета служит обязательным условием успешного лечения язвенного колита. При остром течении или тяжелом обострении рекомендуют первые 2—4 сут ограничиться чаем с сухарями.
Салазопрепараты в лечении колита
Салазопрепараты используются при всех формах и типах течения неспецифического язвенного колита . Однако их место в системе его фармакотерапии бывает неравноценным. Им принадлежит главенствующая роль при легкой и отчасти среднетяжелой форме НЯК. Этому обычно соответствует дистальная или левосторонняя локализация язвенного процесса. При остром же течении болезни или ее тяжелой форме изолированное применение салазопрепаратов лишь иногда приносит успех. Из отдельных представителей рассматриваемых средств длительное время вне конкуренции находился салазосульфапиридин. Он и сейчас не утратил своего значения. Перед назначением салазосульфапиридина, как и других салазопрепаратов, надо убедиться в отсутствии лейкопении, а в процессе лечения каждые 7—10 сут контролировать уровень лейкоцитов в крови.
Первые сутки Салазосульфапиридин больной принимает по 0,5 г 4 раза в день после еды, на следующий день дозу удваивают, а в дальнейшем при хорошей переносимости доводят до 6—8 г. Это, однако, удается далеко не всегда из-за возникающих побочных реакций, главным образом в виде тошноты, рвоты, анорексии и головной боли.
Литературные сведения о подходе к определению оптимальной дозировки Салазосульфапиридина отличаются разнообразием. М. X. Левитан и соавт. (1980) рекомендуют исходить из тяжести заболевания. При легких формах доза составляет 2—4 г, при среднетяжелых — 4—6 г, а при тяжелых повышается до 10—12 г/сут салазосульфапиридина, но с последним вряд ли можно согласиться. Так, A. Khan и соавт. (1980) призывают ограничиваться 2 г/сут, считая, что уже назначение 4 г/сут данного препарата чревато опасностью побочных явлений. По нашему опыту дозы целесообразно подбирать от малого к большему, ориентируясь на достигаемый эффект и переносимость. Надо иметь в виду, что последняя нередко ухудшается вместе с увеличением тяжести болезни. Большей частью дозировка остается в пределах 4—6 г/сут, поскольку превышающая ее часто вызывает побочные реакции.
Основной курс лечения занимает приблизительно 6—8 нед, но нередко оказывается более длительным. По мере стихания активности болезни дозу салазосульфапиридина снижают до 1,5-2 г/сут. Эта или несколько меньшая доза (1 г/сут) используется для поддерживающей, предупреждающей рецидивы НЯК терапии. Ее минимальная длительность, видимо, должна составлять около 1 года, но некоторые авторы увеличивают данный срок
Лекарства нового поколения при язвенном колите
В последние годы Cалазосульфапиридин стал использоваться реже. Сейчас чаще прибегают к более новым салазопрепаритам:>Cализопиридазину и Cалазодиметоксину. Они применяются в меньших дозах и лучше переносятся. При обострении язвенного колита тот и другой назначают по 0,5 г 4 раза в день после еды. Cалазодпметоксин при тяжелом течении болезни может назначаться и по 4 г/сут. По мере стихания обострения дозу снижают с тем, чтобы перейти к поддерживающему лечению. При нем один из упомянутых препаратов назначают по 0,5 г 1—2 раза в сутки.
Салазопиридазин может применяться также местно в виде 5% суспензии. Ее слегка подогревают и вводят в прямую кишку по 20—40 мл 1—2 раза в сутки.
Эту суспензию, а также свечи, содержащие 1 г Салазопиридазина, используют преимущественно при дистальных формах язвенного колита.
Не столь давно установлено, что действующим началом салазопрепаратов является 5-аминосалиииловая кислота (5-АСК), тогда как сульфаниламидный компонент лишен существенного лечебного значения. Больше тою, он расценивается как главный источник побочных аффектов [Dorner W., 1986]. Широкому применению 5-аминосалициловой кислоты препятствует ее нестойкость. Однако это преодолимо.
За рубежом под названиями Асакол, Салофальк и Месалазин выпускаются лекарства от колита этой кислоты с защитным покрытием. Асакол содержит 400 мг 5-АСК, снабжен акриловым покрытием, которое разрушается при рН свыше 7, т. е. препарат может достигать восходящей кишки. Другой представитель 5-АСК — салофальк, содержащий 250 мг активного вещества, защищен, помимо акрилового покрытия, полунепроницаемой оболочкой из этил целлюлозы. Они разрушаются при рН выше 5,6, т. е. их действие ограничивается дистальными отделами тонкой кишки. По данным F. Martin (1987), Асакол лучше назначать больным, страдающим неспецифическим язвенным колитом, а Салофальк — болезнью Крона. Таблетки по I—2 штуки принимают 2—3 раза в день. Эффект примерно соответствует таковому Салазосульфапиридина, но побочные явления наблюдаются реже.
W. Dorner, (1986). М. МсРпес и соавт. (1987) показали высокую эффективность лечебных микроклизм с 5-АСК (в дозе 4 г , растворенных в 60 мл жидкости), а также свечей у больных с язвенным проктосигмоидитом, прослеженных в сроки от 3 мес до 3 лет. Лечение оказалось успешным у 87% больных. Редкими побочными проявлениями служили обострения геморроя и пери-анальные повреждения. Применение 5-АСК в течение 2 нед оказалось более эффективным, чем аналогичное введение 100 мг Гидрокортизона.
Важно, что с помощью радиоактивной метки «Ее удалось установить миграцию лекарственного средства вверх по кишке, что позволяет применять его при более распространенных формах данного заболевания [Ctiiiipiir; Л. et cil., 1987]. Наряду с этим предлагаются препараты, в которых 5-аминосалициловая кислота соединена не с сульфаниламидами, а с другими веществами. Сюда, например, относятся Олсалазин, представляющий азосоединение 2 молекул 5-аминосалициловой кислоты. В дозе 2 г 4 раза в день он оказался эффективным у 40% больных НЯК [Selby W. et al., 1985]. Этот пр